Foram encontradas 60 questões.
As usinas nucleares de Angra 1 e 2 apresentam menor risco de acidentes quando comparadas à usina de Chernobyl, palco do maior acidente nuclear da história, que ocorreu na cidade de Prypiat, norte da Ucrânia, em 1986. A maior diferença reside no sistema de refrigeração que utiliza a égua do mar, destinado a evitar o incêndio no reator, como ocorreu no grande acidente de Chernobyl. No entanto, a técnica mais segura causa impacto ambiental à vida marinha próxima a usina, pois:
Provas
Uma amostra de 9,5682g de aço (ferro-carbono) foi tratada com ácido clorídrico a 1 mol L-1 em volume o suficiente para consumir todo o analito. Sob condições normais de temperatura e pressão, o volume total de hidrogênio formado foi de 3,380 L. Dessa forma, o teor de ferro na amostra é de aproximadamente:
Provas
A diferença de potencial padrão de uma pilha (ddp) depende exclusivamente do tipo de eletrodos escolhidos. De acordo com os potenciais de redução listados abaixo, a pilha que apresenta a maior ddp pode ser representada como:

Provas
A equação de Arrhenius foi desenvolvida no final do século XIX e está representada abaixo:
!$ k = Ae^{-Ea/RT} !$
Essa equação relaciona a constante de velocidade com a temperatura e cria um parâmetro cinético, a Energia de Ativação, que a Termodinâmica interpreta como:
Provas
A espectroscopia e a difração de raio X são técnicas fundamentais para determinar os ângulos de ligação que, por sua vez, auxiliam na classificação da geometria molecular, Contudo, para moléculas pequenas, a Teoria da Repulsão do Par de Elétrons da Camada de Valências pode prever, com boa precisão, as estruturas. O tetrafluoreto de enxofre, usado na fabricação de organofluorados, por exemplo, apresenta a geometria:
Provas
Considere o equilíbrio químico entre o N2O4 e o NO2:
N2O4(g) → 2 NO2(g) K = 0,2 !$ \Delta H = +58,0 kJ/mol !$
Com o aumento da temperatura e a diminuição da pressão total do sistema, a nova constante K, após atingir um novo equilíbrio químico, será:
Provas
A obtenção do ferro se dá na reação entre o minério de ferro, o óxido de ferro II (MM = 71,8 g/mol) e o monóxido de carbono, de acordo com a seguinte equação:
FeO(s) + CO(g) → Fe(s) + CO2(g)
Considerando as equações termoquímicas de outros minérios de ferro, como a hematita, a magnetita e a wusita, a entalpia de obtenção do ferro, a partir 215,4 g de óxido de ferro, é igual a:
Fe2O3(s) + 3CO(g) → 2 Fe(s) + CO2(g)
!$ \Delta H_1 = -25 kJ/mol !$
3FeO(s) + CO2(g) → Fe3O4(s) + CO(g)
!$ \Delta H_2 = -36 kJ/mol !$
2 Fe3O4(s) + CO2(g) → 3 Fe2O3(s) + CO(g)
!$ \Delta H_3 = +47 kJ/mol !$
Provas
Ao planejar uma síntese orgânica, é necessário conhecer as propriedades físico-químicas dos reagentes envolvidos na reação, para propor a melhor rota e os mecanismos. Uma dessas propriedades é a basicidade dos compostos, que indica a habilidade de a molécula receber o próton e formar um produto estável. Dentre as moléculas a seguir, aquela que forma o produto mais estável em uma reação ácido base é a:
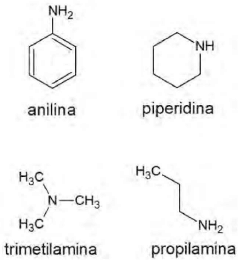
Provas
As sucessivas ionizações no nitrogênio e suas respectivas energias de ionização estão representadas no gráfico abaixo:
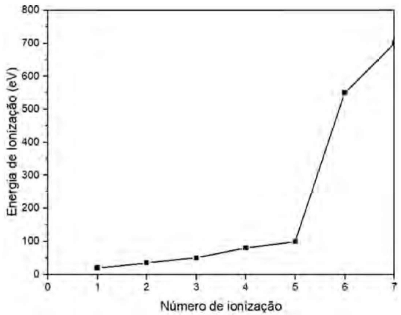
A grande variação de energia que ocorre entre a quinta ionização e a sexta ionização é devido:
Provas
A Morina é um substrato orgânico modelo, utilizado para avaliar a capacidade alvejante em processos de branqueamento. Essa avaliação pode ser feita através do decaimento de sua banda em 390 nm, em uma cu beta de 2 mL, em um espectrofotômetro. A concentração ideal da Morina na cubeta é de 5 x 10-5 mol L-1 para evitar o limite máximo de detecção dos aparelhos. Se 200 µL provenientes de uma solução mãe estocada em um balão volumétrico de 100 mL são adicionadas à cubeta (volume total 2 mL), a massa necessária de Morina para preparar a solução mãe, considerando a concentração final ideal, é de:
(Massa Molar Morina = 302,23 g/mol)
Provas
Caderno Container