Foram encontradas 60 questões.
O sulfito monoácido de sódio NaHSO3 é um importante insumo nas indústrias de papel e couro. Ele pode ser obtido a partir da seguinte equação:
![]()
O volume de SO2 (em litros) necessário para reagir com 424 g de carbonato de sódio é
Dado: Volume molar = 24,5 L (P = 1atm e T = 25ºC)
Provas
O selênio é um micronutriente que se apresenta na forma do ânion seleneto (Se2-) em proteínas, leguminosas e cereais. Uma marca de atum sólido em lata apresenta a concentração de seleneto equivalente a 39,5 μg/100g.
Ao ingerir 20 g desse atum, a quantidade de seleneto é, aproximadamente,
Provas
O Biogás apresenta teores de sulfeto de hidrogênio que corroem tubulações metálicas. Uma das estratégias de remoção de sulfeto consiste na reação não balanceada abaixo:
![]()
Considerando que a concentração de sulfeto de hidrogênio em um determinado biogás é de 3,40 g/L, determine a massa aproximada obtida de sulfeto de ferro III ao reagir completamente com 100 L desse biogás.
Provas
Para o equilíbrio genérico: A ⇌ B, temos:
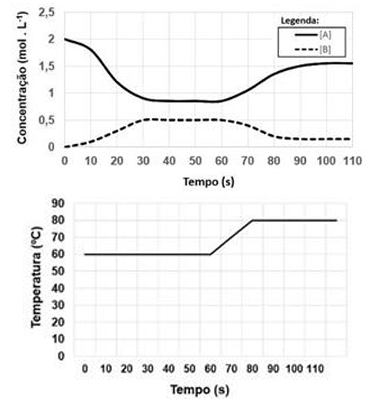
Com base na análise dos gráficos, assinale a opção correta.
Provas
O Teste de Harger - desenvolvido na década de 1930 - foi largamente utilizado como bafômetro antes da evolução dos etilômetros eletrônicos. No procedimento, a pessoa assoprava em um balão conectado a um tubo contendo dicromato de potássio em meio ácido. Abaixo a reação que ocorre quando o ar expirado continha etanol.
![]()
O agente oxidante, o agente redutor e o valor do somatório dos menores coeficientes inteiros que realizam o balanceamento de massa e de carga da equação são, respectivamente,
Provas
O arranjo molecular é a forma como as nuvens eletrônicas se dispõem em torno do átomo central. Já a geometria, pode ser definida a partir da posição ocupada pelos átomos ligantes.
Assim sendo, a geometria da molécula de pentacloreto de fósforo (PCl5) é
Provas
Na figura a seguir, temos a representação de um átomo - fora de proporção - de acordo com o modelo de Bohr.
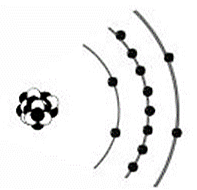
Considerando a regra do octeto, assinale a opção que apresenta o único elemento que se combina com esse átomo para formar um composto iônico com fórmula mínima de proporção, 1 cátion : 1 ânion.
Provas
A tabela abaixo mostra algumas propriedades relacionadas a três elementos químicos:
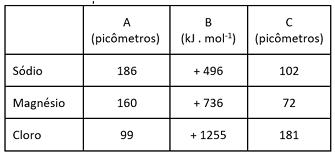
As propriedades A, B e C correspondem, respectivamente, a
Provas
Ernest Rutherford coordenou, em 1911, um experimento em seu laboratório que consistiu em bombardear uma finíssima lâmina de ouro com partículas alfa (He2+), emitidas por um elemento radioativo. Duas observações principais estão descritas abaixo:
I. a maioria das partículas α atravessava a lâmina de ouro sem sofrer desvios ou sofrendo desvios muito pequenos;
II. 0,01% das partículas alfa eram desviadas para ângulos maiores do que 90°.
Com base nessas observações, Rutherford pôde concluir que:
Provas
"Ela produzia luminescência em certos materiais fluorescentes, sensibilizava chapas fotográficas, mas em si era invisível ao olho humano [...]. Não se tratava de luz (por ser invisível e atravessar grandes espessuras de madeira ou papel), não era igual aos raios catódicos (não sofria desvio com ímãs e tinha poder de penetração muito superior), nem aos raios ultravioleta ou infravermelho (pelo seu poder de penetração)"
Roentgen, W. C.; Annalen der Physik und Chemie 1895
Roentgen assim descreve algumas propriedades da radiação que acabara de descobrir: os Raios X.
O modelo atômico que não consegue, sob nenhuma hipótese, propor uma explicação sobre a origem desses raios é o de
Provas
Caderno Container