Foram encontradas 80 questões.
O teor de ferro em uma amostra de minério de ferro pode ser determinado por Espectrometria de Absorção Molecular (EAM) na região do visível, com base na seguinte reação:
Fe 3+ + SCN- --> Fe(SCN)6 3-Para análise de uma amostra de minério de ferro por EAM, 2 g da mesma foram adequadamente abertos, transferidos para um balão volumétrico de 1 L, que foi completado com água, de maneira a preparar uma solução contendo 2 g de minério/L. Dessa solução, pipetou-se 1 mL para outro balão de 1 L, adicionou-se 20 mL de uma solução de ZnSO4, 10 mL de H2O2 10 Vol., 200 mL de uma solução de KSCN, e completou-se o volume com água, produzindo o que se chamou de solução diluída de amostra. Uma série de padrões foi preparada a partir de uma solução estoque intermediária de 100 μg/mL de Fe 3+ , pipetando-se 1, 2, 3, 4 e 5 mL da mesma para 5 balões volumétricos de 100 mL, adicionando-se a cada balão 2 mL de solução de ZnSO4, 1 mL de H2O2 10 Vol., 20 mL de uma solução de KSCN e completando-se o volume com água, produzindo os padrões 1, 2, 3, 4 e 5, respectivamente. As absorbâncias para os padrões, lidas em um Espectrofotômetro de Absorção Molecular, no comprimento de onda 510 nm, estão apresentadas abaixo:

A curva de calibração, construída a partir dos padrões, está representada no gráfico abaixo, bem como sua equação.
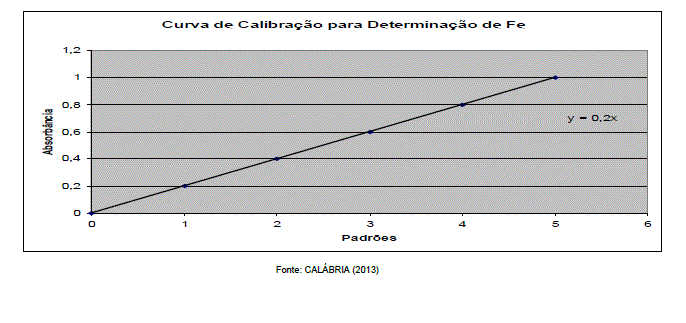
Provas
A corrosão é a destruição ou deterioração de um material devido à reação química ou eletroquímica com seu meio. Pinturas e revestimentos ajudam a minimizar esse desgaste. A galvanização consiste em uma proteção eficiente para tubulações de aço, em que uma camada de zinco é aplicada sobre a superfície da liga metálica. Essa camada minimiza a ação da água e do oxigênio sobre o aço.
Dados :
Fe 2+ (aq) + 2e - --> Fe (s) E0 /V = - 0,44
Zn 2+ (aq) + 2e - --> Zn (s) E0 /V = - 0,76
Sobre a galvanização, pode-se afirmar que:
Provas
Um técnico pretende preparar 500,00 mL de uma solução de H2SO4 de concentração igual a 1 eq.g.L-1. O volume de reagente, em mL, que deve ser transferido para o balão volumétrico é de:
Dados: Pureza = 100% m/m e ρ = 2,000 g.cm-3
Provas
Um técnico de laboratório precisa identificar o conteúdo de três frascos rotulados A, B e C.
Sabe-se que os frascos contêm tolueno, pentano e hexeno, não necessariamente nessa ordem. Após realizar diversas análises, ele obteve os seguintes resultados:
I - O conteúdo do frasco A reagiu com permanganato de potássio em meio básico, a frio e foi identificado com pentano;
II - O conteúdo do frasco B não descorou uma solução de bromo em tetracloreto de carbono (na ausência de luz e em temperatura ambiente) e foi identificado como hexeno;
III- O conteúdo do frasco C reagiu com a N-bromossuccinimida (na presença de luz), formando brometo de benzila como produto principal, e foi identificado como tolueno.
Está(ão) CORRETA(S) :
Provas
Em relação às vidrarias utilizadas em um laboratório de Química, considere as afirmações:
I - O tubo de ensaio é empregado para fazer reações em escala reduzida.
II - O funil de separação é utilizado na extração líquido/líquido.
III- Pipetas volumétricas são utilizadas para medir volumes variáveis.
IV- O erlenmeyer é uma vidraria calibrada para medir o volume de líquidos de forma precisa.
Estão CORRETAS:Provas
Em um laboratório de Química, é primordial que o aluno assuma uma postura cuidadosa e responsável durante as experiências. Esses cuidados têm o objetivo de evitar acidentes, garantir análises seguras e diminuir o gasto dos reagentes.
Com relação ao enunciado, considere as proposições a seguir:
I - Sempre que for necessário diluir um ácido concentrado, deve-se adicionar, lentamente e com agitação, a água sobre o ácido, nunca o contrário.
II - No aquecimento de um tubo de ensaio, contendo qualquer substância, não voltar a extremidade aberta do tubo para si ou para outra pessoa próxima.
III- As sobras dos reagentes devem ser transferidas para os respectivos frascos estoques.
IV- Ácidos e bases (mesmo diluídos) devem ser manuseados com muito cuidado. Se tocarem a pele, lavar o local, demoradamente, com água corrente e, em seguida, com um antídoto: para bases, usar vinagre ou sumo diluído de limão e para ácidos, usar solução de bicarbonato de sódio, NaHCO3(aq).
Estão CORRETAS:
Provas
- Química OrgânicaFunções Oxigenadas: Álcool, Fenol e Enol
- Química OrgânicaReações OrgânicasReações Orgânicas: Oxidação, Redução e Polimerização
Os alcoóis são compostos versáteis e podem ser usados como material de partida para a preparação de uma grande variedade de compostos. Sobre os alcoóis, analise as proposições a seguir:
I - Não ocorre oxidação do CH3-C(CH3)OH-CH3 em presença de dicromato de potássio em meio ácido.
II- A desidratação intermolecular, que ocorre entre 2 moléculas de etanol a 140°C, em presença de H2SO4 , gera buteno-2.
III- A reação do butanol terciário, com o reativo de Lucas (HCl/ZnCl2), processa-se imediatamente.
Está(ão) INCORRETA (S):
Provas
Um químico fracionou uma mistura contendo as três substâncias representadas pelas fórmulas estruturais abaixo, utilizando a técnica de cromatografia por adsorção em coluna. No procedimento realizado foi utilizada sílica como adsorvente.
Ao percolar a coluna com os solventes A, B e C, que formam uma série eluotrópica, verificou que a primeira fração continha o composto X, a segunda fração, o composto Y, e a última fração, o composto Z. O sistema de solventes a seguir, que foi usado como fase móvel para justificar a ordem de eluição encontrada, é:
Solvente A Solvente B Solvente CProvas
De acordo com a legislação vigente, a cachaça é uma aguardente com graduação alcoólica entre 38% a 48%, obtida pela destilação do mosto fermentado do caldo de cana-de-açúcar e produzida no Brasil. A cachaça contém água, etanol e pequenas quantidades de outras substâncias, dentre as quais o ácido acético e acetato de etila, que são formados, a partir do etanol, respectivamente, por reações de:
Provas
Em laboratórios de Química Orgânica, é muito comum a realização de reações de oxidação para identificar se determinada substância é um aldeído ou uma cetona. Entre os oxidantes que costumam ser usados, estão os reativos de Tollens, Fehling e Benedict. Aldeídos e cetonas podem ser diferenciados quando se utiliza de maneira adequada o reagente:
Provas
Caderno Container