Foram encontradas 60 questões.
A poluição atmosférica causada pelo gás dióxido de nitrogênio (NO2) é uma das causas de destruição da camada de ozônio. A reação deste gás com o ozônio é 2NO2 + O3 ⇌ N2O5 + O2. Admitindo-se que a velocidade de formação do N2O5 é de 0,06 mol/min, a massa, em gramas, de dióxido de nitrogênio consumida em 1h tem o valor aproximado de
Provas
Questão presente nas seguintes provas
A respeito do processo de recristalização, o técnico em química deve observar algumas características, exceto
Provas
Questão presente nas seguintes provas
Considere a reação ácido-base que ocorre em uma titulação de 50 mL de ácido clorídrico (HCl) de concentração 0,1mol/L com uma solução de hidróxido de sódio (NaOH) 0,2 mol/L. O valor do pH, quando o volume da solução de NaOH for de 10mL, é
Considere Log2 = 0,3; Log3 = 0,5 e Log5 = 0,7.
Provas
Questão presente nas seguintes provas
A concentração de cloreto de sódio na água do mar é 0,08 mol/L. Com a finalidade de preparar 20 litros desta solução, misturaram-se 2 litros de uma solução de cloreto de sódio 0,5 mol/L com outra X mol/L. O valor aproximado de X é
Provas
Questão presente nas seguintes provas
Sabe-se que a tirosina é uma substância participante do processo de síntese de proteínas. A sua fórmula estrutural está representada abaixo:
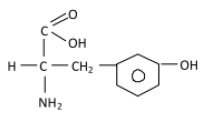
Assim, as funções orgânicas presentes em sua molécula são
Provas
Questão presente nas seguintes provas
As equações químicas abaixo representam fenômenos químicos.
(1) NaCl(aq) + AgNO3(aq) → AgCl(s) + NaNO3(aq)
(2) Na2CO3(aq) + HCl(aq) → NaCl(aq) + CO2(g) + H2O(l)
(3) CO(g) + FeO(s) → Fe(l) + CO2(g)
As evidências que indicam o acontecimento de um fenômeno químico são, respectivamente,
Provas
Questão presente nas seguintes provas
Peças metálicas podem ser protegidas com outro metal, para servir como metal de sacrifício.
Considere os metais e seus respectivos potenciais-padrão.
Mg2+ + 2e- → Mg E0 = -2,37 V
Al3+ + 3e- → Al E0 = -1,66 V
Co2+ + 2e- → Co E0 = -0,28 V
Pb2+ + 2e- → Pb E0 = -0,13 V
Cu2+ + 2e- → Cu E0 = + 0,34 V
Ag+ + 1e- → Ag E0 = +0,80 V
Para uma peça de alumínio, pode servir de metal de sacrifício:
Provas
Questão presente nas seguintes provas
Uma solução, com 588,0 g de ácido sulfúrico, H2SO4, por litro de solução, tem densidade de 1,3 g/cm³. A porcentagem em massa, a molalidade e a concentração em quantidade de matéria nessa solução são, aproximadamente,
Provas
Questão presente nas seguintes provas
Considere os quatro manômetros que se seguem. Sobre cada coluna de mercúrio, há 1 mL de soluções 1 molal dos compostos: ureia, que é um composto molecular de fórmula (NH2)2CO, NaCl, CaBr2 e Al2(SO4)3. Considere a dissociação total dos eletrólitos. As soluções X, Y, Z e K são, respectivamente,
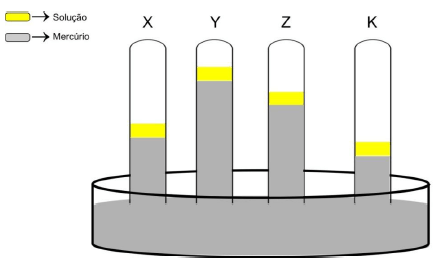
Provas
Questão presente nas seguintes provas
20 mL de ácido nítrico (HNO3) de concentração 0,2 mol/L foram adicionados a 32 mL de uma solução de hidróxido de sódio (NaOH) de concentração desconhecida. Se o pH obtido foi igual a 10, a concentração da solução de NaOH tem um valor aproximado de
Considere a temperatura de 25ºC, Kw = 10-14.
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container