Foram encontradas 40 questões.
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
A pedido do professor de química, um técnico de laboratório preparou uma solução de sulfato de potássio. Para isso, dissolveu 8,7 g do sal em água e completou o volume para 100 mL utilizando um balão volumétrico. Diante dessa informação, assinale a alternativa que apresenta a concentração aproximada, em mol/L, da solução de sulfato de potássio obtida.
Provas
Determinada reação química ocorre espontaneamente no sentido de formação dos produtos, sob temperatura e pressão constantes, embora ainda não tenha atingido o equilíbrio químico. Considerando o estado descrito, assinale a alternativa correta quanto à variação de energia livre de Gibbs da reação (ΔG) e ao valor do quociente da reação (Q), considerando K como a constante de equilíbrio.
Provas
No contexto das reações orgânicas, considere a adição eletrofílica clássica do HBr ao 2-metilpropeno. Assinale a alternativa que apresenta corretamente o composto orgânico obtido como produto principal dessa reação.
Provas
Em qual das seguintes equações químicas, considerando a temperatura constante, o equilíbrio se desloca no sentido de formação de mais produto(s) como resultado da diminuição do volume total, provocada pelo aumento da pressão do sistema?
Provas
Em uma célula eletrolítica, sob temperatura constante, uma corrente elétrica contínua de 6,7 A é aplicada a uma solução contendo íons Cu2+(aq) durante 1 hora, resultando na deposição de cobre metálico no cátodo. Considerando que apenas os íons Cu2+(aq) são reduzidos, assinale a alternativa que apresenta, de forma aproximada, a massa de cobre depositada.
Dado: Constante Faraday (F) = 96480 C/mol elétron.
Provas
Assinale a alternativa que apresenta a molécula com momento dipolar diferente de zero.
Provas
O isótopo tório-232 \((^{232}_{90}Th)\) é um elemento radioativo que sofre um processo de decaimento por emissão de uma partícula alfa (α), transformando-se em um nuclídeo mais estável. Com base nesse processo de decaimento, os números de prótons e nêutrons do nuclídeo formado são, respectivamente,
Provas
Em uma aula experimental de cinética química, conduzida pelo professor de química, foi possível determinar a lei de velocidade da seguinte reação:
NO(g) + ½ O2(g) → NO2(g)
Sabe-se que a reação é de primeira ordem em relação ao NO e de terceira ordem global. Diante dessas informações, analise as assertivas e assinale a alternativa que aponta a(s) correta(s).
I. A lei de velocidade da reação é: v = k [NO] [O2]2 .
II. Se a concentração de NO for aumentada em um fator de 1,5, mantendo a concentração de O2 constante, a velocidade da reação aumenta em um fator de 0,75.
III. Se a concentração de O2 for aumentada em um fator de 1,5, mantendo a concentração de NO constante, a velocidade da reação aumenta em um fator de 2,25.
Provas
Considere a fórmula estrutural da molécula orgânica a seguir:
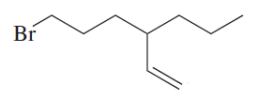
Com base nessa estrutura, assinale a alternativa que apresenta o nome oficial correto da molécula de acordo com as regras da IUPAC.
Provas
Em relação à propriedade periódica denominada energia de ionização, assinale a alternativa INCORRETA.
Provas
Caderno Container