Foram encontradas 230 questões.
O Brasil já possui quase 5.000 tipos de agrotóxicos liberados pelo governo federal, por meio do Ministério da Agricultura, Pecuária e Abastecimento. Leia, a seguir, uma notícia veiculada sobre a liberação de agrotóxicos em 2021.
|
APÓS NOVO RECORDE, BRASIL ENCERRA 2021 COM 562 AGROTÓXICOS LIBERADOS, SENDO 33 INÉDITOS Registros de defensivos cresceram 14% em relação a 2020. Aprovações vêm aumentando desde 2016. O Brasil encerrou 2021 com 562 agrotóxicos liberados, maior número da série histórica iniciada em 2000 pelo Ministério da Agricultura. Ainda em dezembro, o total de aprovações já tinha superado o recorde de 2020. As últimas liberações de 2021 foram publicadas em janeiro no Diário Oficial da União (DOU). O volume foi 14% superior ao de 2020, quando 493 pesticidas foram autorizados. Os registros vêm crescendo ano a ano no país desde 2016. |
https://g1.globo.com/economia/agronegocios/noticia/2022/01/18/apos-novo-recorde-brasil-encerra-2021-com-562-agrotoxicos-liberados-sendo-33-ineditos.ghtml
O glifosato é o agrotóxico mais vendido no Brasil. Ele é um herbicida sistêmico de amplo espectro e dessecante de culturas. Suas fórmulas estrutural e molecular são apresentadas abaixo:
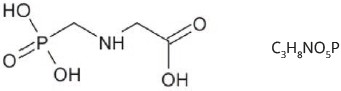
Considerando a estrutura apresentada, a alternativa que contém corretamente as funções orgânicas presentes na sua estrutura molecular é:
Provas
A Lei de Faraday da eletrólise enuncia que “a quantidade do produto formado ou do reagente consumido por uma corrente elétrica é estequiometricamente equivalente à quantidade de elétrons fornecidos”. Pode-se afirmar, portanto, que a quantidade (em mols) de Al(s) que pode ser produzida a partir do alumínio no composto Al2O3, se 5 mols de elétrons forem fornecidos, é aproximadamente:
(ATKINS; JONES, Princípios de Química: questionando a vida moderna e o meio ambiente, Editora Bookman, 2006)
Provas
“A meia-vida, t1/2, de uma substância é o tempo necessário para que sua concentração caia à metade do valor inicial”. A figura abaixo mostra a concentração do cloreto de butila (C4H9Cl) como uma função do tempo:
(ATKINS; JONES, Princípios de Química: questionando a vida moderna e o meio ambiente, Editora Bookman, 2006)
Variação da Concentração com o Tempo
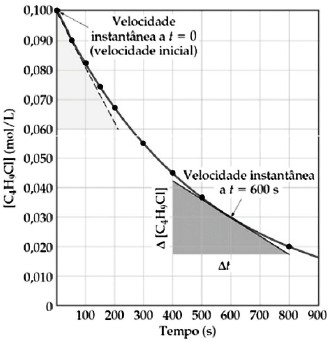
Fonte: BROWN; LEMAY; BURSTEN, Química: a ciência central, São Paulo: Pearson Prentice Hall, 2005, p. 487
Pode-se concluir, observando o gráfico, que a meia-vida da reação de C4H9Cl com água ocorre aproximadamente no tempo de:
Provas
“A energia livre de Gibbs é uma grandeza termodinâmica notável”. A entropia é considerada uma função de estado assim como a entalpia. Considerando a síntese da amônia a partir de N2(g) e H2(g) a 298 K conforme equação a seguir:
(BROWN; LEMAY; BURSTEN, Química: a ciência central, São Paulo: Pearson Prentice Hall, 2005, p. 702)
N2(g) + 3 H2(g) → 2 NH3(g)
E conhecendo as informações do quadro abaixo:
| Substância | !$ \Delta !$Hºf (kJ.mol-1) | Sº (J.mol-1.k-1) |
| N2 (g) | 0 | 191,5 |
| H2 (g) | 0 | 130,6 |
| NH3 (g) | - 80,3 | 111,3 |
Podemos afirmar, com base nos dados apresentados, que o valor da variação da energia livre de Gibbs para a síntese da amônia, em kJ.mol-1, é aproximadamente:
Provas
A reação entre 0,20 mol.L-1 de N2 (g) com 0,20 mol.L-1 de H2 (g) resulta em 0,60 mol.L-1 de NH3 (g) quando atingido o equilíbrio químico. Considerando que a reação química ocorre em condições normais de temperatura e pressão, assinale a alternativa que indica o valor correto da Constante de equilíbrio em função da concentração (Kc) nessas condições.
Considere a equação química não balanceada: N2 (g) + H2 (g) ↔ NH3 (g)
Provas
O preparo de soluções é uma das práticas mais comuns e importantes nos laboratórios de química. Soluções podem ser preparadas a partir de um soluto sólido ou a partir de uma solução concentrada em estoque desse soluto. Considere uma solução de nitrato de prata (AgNO3) em estoque que possui percentual em massa de 70% e densidade de 4,35 g.mL-1. Dada a massa molar: AgNO3 = 170 g.mol-1, para preparar 250 mL de uma solução aquosa de AgNO3 com concentração de 0,2 mol.L-1, é necessário retirar um volume da solução estoque de:
Provas
A teoria de Arrhenius para ácidos e bases é baseada da dissociação eletrolítica dos íons hidrogênio e hidroxila em meio aquoso. No entendimento de Arrhenius, as bases são compostos que, quando dissolvidos em água, aumentam a concentração de íons OH-. Essa teoria/definição explica apenas alguns fenômenos básicos (quando dissolvidos em água), porém não explica quando envolvidas substâncias em soluções não aquosas. De acordo com a teoria mais abrangente existente, as bases são compostos que doam um par de elétrons. Qual/is foi/foram o(s) cientista(s) proponente(s) de tal definição?
(BROWN, Theodore L. Química, a ciência central. São Paulo: Prentice Hall, 2005)
Provas
Substâncias ácidas são caracterizadas pelo sabor azedo, e geralmente exalam um cheio forte e irritante, ou ainda desagradável e pungente. Dentre as teorias/definições mais conhecidas sobre os ácidos, estão as propostas por Svante Arrhenius, por Johannes Bronsted e Thomas Lowry e por Gilbert Newton Lewis. Analise cada descrição a seguir:
I - Os ácidos são moléculas ou íons doadores de prótons (teoria protônica ou de pares ácido-base conjugados).
II - Os ácidos são compostos que, quando dissolvidos em água, aumentam a concentração de íons hidrogênio H+ em solução (teoria da dissociação eletrolítica).
III - Os ácidos são moléculas ou íons doadores de um par de elétrons (teoria relacionada ao par de elétrons).
IV - Os ácidos são compostos que atuam como receptores de um par de elétrons (teoria relacionada ao par de elétrons).
V - Os ácidos são compostos que atuam como receptores de prótons (teoria protônica ou de pares ácido-base conjugados).
A relação CORRETA entre as definições existentes e seus respectivos proponentes consta na alternativa:
Provas
As interações intermoleculares (forças) influenciam a química de muitas formas, pois são cruciais na determinação e configuração de estruturas de moléculas biologicamente importantes, como o DNA e as proteínas. As proteínas são moléculas de elevado peso molecular, sintetizadas pelos organismos vivos por meio da condensação de um grande número de aminoácidos. A ligação entre o grupo carboxila de um e o grupo amina de outro aminoácido é covalente, também conhecida como ligação peptídica. As proteínas apresentam estruturas primárias, secundárias, terciárias e quaternárias. Sobre as interações intermoleculares que dão estabilidade para a estrutura terciária, a alternativa CORRETA é:
(KOTZ, J. C.; TREICHEL, P. M.; TOWNSEND, J. R.; TREICHEL, D. A.; Química Geral e Reações Químicas, 3. ed.; São Paulo: Cengage Learning, 2016)
Provas
Observe as seguintes afirmações sobre as condições para a ocorrência de reações químicas:
I - É necessário haver afinidade química entre os reagentes.
II - As colisões precisam ser favoráveis entre suas moléculas.
III - É necessário que a barreira energética dos reagentes seja superada por meio da Energia de ativação.
IV - Menor superfície de contato entre reagentes facilita as colisões.
Qual a alternativa CORRETA?
Provas
Caderno Container