Foram encontradas 40 questões.
Uma amostra contendo 514 mg de C8 H18, um dos componentes da gasolina, foi colocada em um calorímetro com oxigênio suficiente para promover a combustão completa. O calorímetro foi preenchido com 1,8 L de água e a capacidade calorífica do interior do calorímetro (sem água) é 1,06 kJ.°C-1. A reação promove uma variação de temperatura de 2,8 °C.
Dados: Capacidade calorífica molar da água = 75,3 J.°C-1.mol-1.
Massas atômicas: C=12; H=1
Qual é o calor de combustão por mol, aproximado, de C8 H18?
Provas
Considerando a reação de formação do trióxido de enxofre no equilíbrio e sob temperatura e pressão constantes, é correto afirmar que:

Provas
Considere os potenciais padrões de redução apresentados abaixo:
|
Semi-reação de redução |
E°, V |
|
Ce4+(aq) + e- → Ce3+(aq) |
+1,61 |
|
Cℓ2(g) + 2e- → 2Cℓ -(aq) |
+1,36 |
|
Cr2O72-(aq) + 14H+(aq) + 6e- → 2Cr3+(aq) + 7H2O(l) |
+1,33 |
|
Cu2+(aq) + 2e- → Cu(s) |
+0,34 |
|
Fe3+(aq) + e- → Fe2+(aq) |
+0,77 |
|
S(s) + 2H+(aq) + 2e- → H2S(aq) |
+ 0,14 |
|
Pb2+(aq) + 2e- → Pb(s) |
-0,13 |
|
Al3+(aq) + 3e- → Al(s) |
-1,66 |
Atkins, P.; De Paula, J. Físico-química. 10. ed. Rio de Janeiro: LTC, 2017.v. 2.
Identifique nas reações abaixo, a que é classificada como um processo espontâneo.
Provas
Uma reação do tipo 2A(g) + Z(g) →2T(g) foi monitorada variando-se a concentração dos reagentes. A velocidade de formação de T foi medida conforme a tabela abaixo.
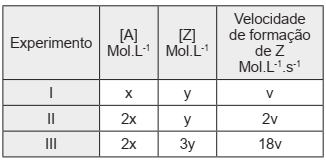
Determine a lei de velocidade e calcule a velocidade da reação em função de v se [A] for x e [Z] for 3y.
Provas
Para determinar o teor de prata em uma liga, realizou-se um procedimento de gravimetria. Tal procedimento partiu de uma amostra da liga de 5g à qual foi submetida a abertura com ácido nítrico seguido de tratamento com solução de cloreto de sódio. Ao fim do procedimento foram obtidos 4,3g de precipitado. A partir dessas informações pode-se constatar que o teor de prata na liga analisada era, aproximadamente, de:
Considere as seguintes massas molares em g. mol-1: Na = 23, Cℓ = 35, Ag = 108).
Provas
Pilhas alcalinas geram corrente elétrica por um período de tempo até 50% mais longo do que uma pilha seca do mesmo tamanho. Considere a reação abaixo, que ocorre nas pilhas alcalinas, e indique a alternativa que apresenta corretamente a reação que ocorre no catodo e no anodo.
![]()
Provas
Considere que para a reação de dissociação
![]() , a pressão parcial de E, no equilíbrio,
é 1 bar a 25°C. Calcule a constante de equilíbrio.
, a pressão parcial de E, no equilíbrio,
é 1 bar a 25°C. Calcule a constante de equilíbrio.
Provas
- FundamentosLigações Químicas
- FundamentosPropriedades das Substâncias
- Química InorgânicaGeometria Molecular, Polaridade e Forças Intermoleculares
“O boro forma uma série notável de compostos binários com o hidrogênio – os boranos. Esses compostos incluem o diborano, B2 H6 , e compostos mais complexos, como o decaborano, B10H14”
(JONES, L.; ATKINS, P. Princípios de química: questionando a vida moderna e o meio ambiente. 5. ed. Porto Alegre: Bookman. 2011.p.632)
Moléculas como o diborano são deficientes em elétrons e, por isso, não podemos escrever estruturas de Lewis válidas. Duas ligações B-H-B são formadas na molécula, formando pontes de hidrogênio. Esse padrão de ligação também é visto no hidrogênio protonado (H3 + ), por exemplo. Como são conhecidas ligações como as pontes presentes no diborano?
Provas
O Cloreto de alumínio sólido é um ácido de Lewis muito utilizado nas reações de substituição orgânica.
O valor da entalpia padrão de formação deste ácido de Lewis encontra-se entre:
Dados:
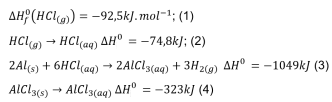
(Fonte: ATKINS, Peter; JONES, Loretta; LAVERMAN, Leroy. Princípios de Química: Questionando a Vida Moderna e o Meio Ambiente. Bookman Editora, 2018)
Provas
- Química OrgânicaReações OrgânicasReações Orgânicas: Substituição, Adição e Eliminação
- Química OrgânicaReações OrgânicasReações Orgânicas: Oxidação, Redução e Polimerização
Provas
Caderno Container