Foram encontradas 50 questões.
Uma balança de dois pratos encontra-se em equilíbrio, como mostra a figura abaixo.
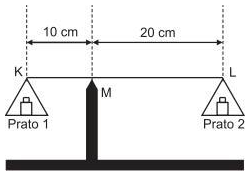
Sabe-se que a massa colocada no Prato 1 é de 1,0 kg, e que os pratos 1 e 2, bem como a barra KL possuem massas desprezíveis.
Qual é, em N, o módulo da força de interação entre o mancal M e a barra KL?
Dado aceleração da gravidade = 10 m/s2

Sabe-se que a massa colocada no Prato 1 é de 1,0 kg, e que os pratos 1 e 2, bem como a barra KL possuem massas desprezíveis.
Qual é, em N, o módulo da força de interação entre o mancal M e a barra KL?
Dado aceleração da gravidade = 10 m/s2
Provas
Questão presente nas seguintes provas
- Química CinéticaRepresentação das Transformações Químicas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
A massa, em g, de K2 Cr2 O7 necessária para o preparo de 400 mL de solução aquosa de dicromato de potássio 0,5 mol L-1 é, aproximadamente, Dado M(K2Cr2O7) = 294 g/mol
Provas
Questão presente nas seguintes provas
Sobre os hidrocarbonetos metano e eteno e os polímeros polietileno e poliestireno, tem-se que:
Provas
Questão presente nas seguintes provas
A água pode ser decomposta como mostra a equação termoquímica a seguir.
H2O(g) → H2(g) + ½ O2(g) ΔHº = 285 kJ
Nessa reação,
H2O(g) → H2(g) + ½ O2(g) ΔHº = 285 kJ
Nessa reação,
Provas
Questão presente nas seguintes provas
A reação do permanganato de potássio com sulfato de estanho II em meio fortemente ácido é representada pela equação não balanceada abaixo.
KMnO4(aq) + SnSO4(aq) + H2SO4(aq) → MnSO4(aq) + Sn(SO4)2(aq) + K2SO4(aq) + H2O( l)
Considere as afirmações abaixo sobre essa reação.
I - MnO4 - é o agente oxidante no meio ácido, e Sn2+ , o agente redutor.
II - No balanço de massa, 2 mol de KMnO4 reagem com 5 mol de SnSO4 .
III - Sn2+ ganha 2 elétrons do MnO4 - ao passar para Sn4+ .
É correto APENAS o que se afirma em
KMnO4(aq) + SnSO4(aq) + H2SO4(aq) → MnSO4(aq) + Sn(SO4)2(aq) + K2SO4(aq) + H2O( l)
Considere as afirmações abaixo sobre essa reação.
I - MnO4 - é o agente oxidante no meio ácido, e Sn2+ , o agente redutor.
II - No balanço de massa, 2 mol de KMnO4 reagem com 5 mol de SnSO4 .
III - Sn2+ ganha 2 elétrons do MnO4 - ao passar para Sn4+ .
É correto APENAS o que se afirma em
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSubstâncias Inorgânicas: dissociação iônica e ionização, conceitos de ácido-base
- Sistemas de EquilíbrioSistemas Homogêneos: Equilíbrio Químico na Água
Ácido etanoico é um ácido muito fraco cuja constante de ionização é Ka = 1,82 x 10-5.
Em meio aquoso, ele se ioniza de acordo com a equação simplificada (I) abaixo.
(I) HC2H3O2(aq)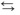 H+(aq) + C2H3O2−(aq)
H+(aq) + C2H3O2−(aq)
Ácido clorídrico é um ácido muito forte e, em meio aquoso, ele se ioniza de acordo com a equação simplificada (II) abaixo.
(II) HCl(aq) → H+(aq) + Cl−(aq)
Na reação da base forte hidróxido de sódio 0,1 mol/L com o ácido etanoico 0,1 mol/L, e com o ácido forte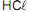 0,1 mol/L, ambos em meio aquoso, ocorrem as seguintes reações:
0,1 mol/L, ambos em meio aquoso, ocorrem as seguintes reações:
(III) NaOH(aq) + HC2H3O2(aq) → NaC2H3O2(aq) + H2O(l)
(IV) NaOH(aq) + HCl(aq) → NaCl(aq) + H2O(l)
Sobre a ionização em (I) e (II) e as reações de neutralização em (III) e (IV), tem-se que:
Em meio aquoso, ele se ioniza de acordo com a equação simplificada (I) abaixo.
(I) HC2H3O2(aq)
Ácido clorídrico é um ácido muito forte e, em meio aquoso, ele se ioniza de acordo com a equação simplificada (II) abaixo.
(II) HCl(aq) → H+(aq) + Cl−(aq)
Na reação da base forte hidróxido de sódio 0,1 mol/L com o ácido etanoico 0,1 mol/L, e com o ácido forte
(III) NaOH(aq) + HC2H3O2(aq) → NaC2H3O2(aq) + H2O(l)
(IV) NaOH(aq) + HCl(aq) → NaCl(aq) + H2O(l)
Sobre a ionização em (I) e (II) e as reações de neutralização em (III) e (IV), tem-se que:
Provas
Questão presente nas seguintes provas
Os nuclídeos 12 C e 13 C
Provas
Questão presente nas seguintes provas
- FundamentosPropriedades das Substâncias
- Química InorgânicaGeometria Molecular, Polaridade e Forças Intermoleculares
- Química InorgânicaSoluções e Substâncias InorgânicasSubstâncias Inorgânicas: dissociação iônica e ionização, conceitos de ácido-base
- Sistemas de EquilíbrioSistemas Homogêneos: Equilíbrio Químico na Água
Um dos produtos da combustão completa da gasolina é o gás carbônico, que é um óxido
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Um técnico preparou duas misturas. A primeira continha glicose totalmente dissolvida em água. À segunda, adicionou amido em água, formando uma mistura que espalha a luz visível incidente.
A respeito dessas misturas, tem-se que
A respeito dessas misturas, tem-se que
Provas
Questão presente nas seguintes provas
Uma amostra de enxofre, obtida de fontes de águas termais, contém 90% em massa de S, e o resto são impurezas inertes. A produção de ácido sulfúrico a partir do enxofre passa pelas seguintes etapas:
S(s) + ½ O2(g) → SO(g)
SO(g) + ½ O2(g) → SO2(g)
SO2(g) + ½ O2(g) → SO3(g)
SO3(g) + H2O(l) → H2SO4(aq)
Considerando rendimento de 80% na formação de ácido sulfúrico a partir do S, a massa, em g, do ácido produzida a partir de 50,0 g da amostra original é, aproximadamente,
S(s) + ½ O2(g) → SO(g)
SO(g) + ½ O2(g) → SO2(g)
SO2(g) + ½ O2(g) → SO3(g)
SO3(g) + H2O(l) → H2SO4(aq)
Considerando rendimento de 80% na formação de ácido sulfúrico a partir do S, a massa, em g, do ácido produzida a partir de 50,0 g da amostra original é, aproximadamente,
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container