Foram encontradas 70 questões.
- Sistemas de EquilíbrioSistemas Homogêneos: Solubilidade dos Sais, Hidrólise dos Sais e Curvas de Titulação.
Uma solução de HC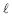 0,0005M foi analiticamente padronizada, titulando-se um volume de 50 mL dessa solução com uma solução 0,001M de NaOH, sendo acompanhado o parâmetro pH durante a adição da solução de NaOH.
0,0005M foi analiticamente padronizada, titulando-se um volume de 50 mL dessa solução com uma solução 0,001M de NaOH, sendo acompanhado o parâmetro pH durante a adição da solução de NaOH.
A curva titulométrica resultante é apresentada no gráfico.
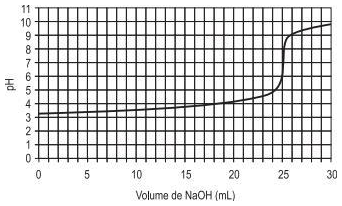
VOGEL, A. I. Análise Química Quantitativa. Rio de Janeiro: LTC, 2002. Adaptado.
Indicador Faixa de pH de mudança de cor
Vermelho de metila 4,2 – 6,3
Verde de bromocresol 3,8 – 5,4
Azul de bromotimol 6,2 – 7,6
Alaranjado de metila 3,1 – 4,4
Fenolftaleína 8,3 – 10,0
Considerando-se os indicadores ácido-base listados após o gráfico, qual o indicador apropriado para a realização dessa análise?
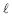 0,0005M foi analiticamente padronizada, titulando-se um volume de 50 mL dessa solução com uma solução 0,001M de NaOH, sendo acompanhado o parâmetro pH durante a adição da solução de NaOH.
0,0005M foi analiticamente padronizada, titulando-se um volume de 50 mL dessa solução com uma solução 0,001M de NaOH, sendo acompanhado o parâmetro pH durante a adição da solução de NaOH. A curva titulométrica resultante é apresentada no gráfico.

VOGEL, A. I. Análise Química Quantitativa. Rio de Janeiro: LTC, 2002. Adaptado.
Indicador Faixa de pH de mudança de cor
Vermelho de metila 4,2 – 6,3
Verde de bromocresol 3,8 – 5,4
Azul de bromotimol 6,2 – 7,6
Alaranjado de metila 3,1 – 4,4
Fenolftaleína 8,3 – 10,0
Considerando-se os indicadores ácido-base listados após o gráfico, qual o indicador apropriado para a realização dessa análise?
Provas
Questão presente nas seguintes provas
- Química OrgânicaFunções Oxigenadas: Álcool, Fenol e Enol
- Química OrgânicaFunções Oxigenadas: Cetona, Aldeído, Éter, Éster, Ácido Carboxílico etc.
Associe as fórmulas condensadas dos compostos orgânicos, dispostas à esquerda, com as respectivas funções, apresentadas à direita.
I – C6 H4 (CH3 )OH
II – C6 H5 CH2 OH
III – C6 H5 COCH3
IV – C6 H5 CH2 COH
P – Álcool
Q – Fenol
R – Cetona
S – Ácido
T – Aldeído
As associações corretas são:
I – C6 H4 (CH3 )OH
II – C6 H5 CH2 OH
III – C6 H5 COCH3
IV – C6 H5 CH2 COH
P – Álcool
Q – Fenol
R – Cetona
S – Ácido
T – Aldeído
As associações corretas são:
Provas
Questão presente nas seguintes provas
- Química OrgânicaFunções Oxigenadas: Álcool, Fenol e Enol
- Química OrgânicaFunções Oxigenadas: Cetona, Aldeído, Éter, Éster, Ácido Carboxílico etc.
Segundo definição da IUPAC, os nomes oficiais dos compostos obtidos quando um átomo de hidrogênio do metanal for substituído por um grupo (–OH) e por um grupo (–OCH3 ), respectivamente, são
Provas
Questão presente nas seguintes provas
- Química CinéticaRepresentação das Transformações Químicas
- Sistemas de EquilíbrioSistemas Homogêneos: Solubilidade dos Sais, Hidrólise dos Sais e Curvas de Titulação.
A 1,0 L de solução de nitrato de prata 1 M, adicionaram-se 146,0 g de ácido clorídrico (329 mL de solução com 37% de HC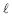 em peso), completando-se com água até um volume final de 2,0 L.
em peso), completando-se com água até um volume final de 2,0 L.
Qual o teor residual de prata na solução?
Dado: Ks AgC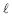 = 1,8 x 10-10
= 1,8 x 10-10
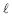 em peso), completando-se com água até um volume final de 2,0 L.
em peso), completando-se com água até um volume final de 2,0 L. Qual o teor residual de prata na solução?
Dado: Ks AgC
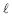 = 1,8 x 10-10
= 1,8 x 10-10Provas
Questão presente nas seguintes provas
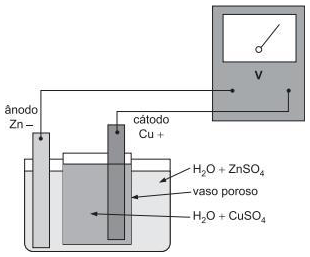
Disponível em: http://www.cis.udel.edu/*portinoi/academic/academic? les/daniellcell.html
A figura acima representa, esquematicamente, uma pilha de Daniel.
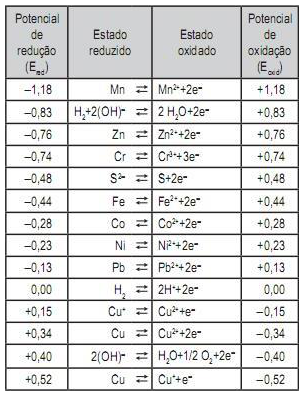
Admitindo-se concentrações (atividades) normais (1,0 M) dos sais, qual a leitura, em V, indicada pelo medidor de força eletromotriz?
Provas
Questão presente nas seguintes provas
As reações químicas envolvem substâncias reagentes e substâncias produtos, conforme as reações abaixo.
Reação 1:
2 Mg(s) + O2 (g) 2MgO(s): reação que acontece em flashes descartáveis de fotografia.
Reação 2:
2NaN3 (s) 3N2 (g) + 2Na(s): reação advinda do acionamento de dispositivos de segurança presentes nos automóveis, chamados airbags. A decomposição do NaN3 (s) origina N2 (g), que os faz inflar.
Reação 3:
Zn(s) + 2HC(aq) ZnC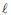 2 (aq) + H2 (g): reação que ocorre quando uma lâmina de zinco é colocada em uma solução aquosa de ácido clorídrico, havendo a formação do ZnC
2 (aq) + H2 (g): reação que ocorre quando uma lâmina de zinco é colocada em uma solução aquosa de ácido clorídrico, havendo a formação do ZnC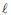 2 (aq) e gás hidrogênio.
2 (aq) e gás hidrogênio.
Reação 4:
BaC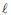 2 (aq) + Na2 SO4 (aq) BaSO4 (s) + 2 NaC(aq): a reação de cloreto de bário com sulfato de sódio produz o cloreto de sódio e o sulfato de bário precipitado.
2 (aq) + Na2 SO4 (aq) BaSO4 (s) + 2 NaC(aq): a reação de cloreto de bário com sulfato de sódio produz o cloreto de sódio e o sulfato de bário precipitado.
Após analisar essas reações, uma estudante de Química fez as seguintes afirmações:
I – As reações 1 e 3 são de “síntese”, e a reação 2 é de “decomposição”.
II – As reações 3 e 4 são, respectivamente, de “simples troca” e de “dupla troca”.
III – A reação 2 é de decomposição.
IV – A reação 1 é de síntese.
Com base na teoria das classificações das reações químicas, a estudante fez afirmações corretas APENAS em
Reação 1:
2 Mg(s) + O2 (g) 2MgO(s): reação que acontece em flashes descartáveis de fotografia.
Reação 2:
2NaN3 (s) 3N2 (g) + 2Na(s): reação advinda do acionamento de dispositivos de segurança presentes nos automóveis, chamados airbags. A decomposição do NaN3 (s) origina N2 (g), que os faz inflar.
Reação 3:
Zn(s) + 2HC(aq) ZnC
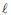 2 (aq) + H2 (g): reação que ocorre quando uma lâmina de zinco é colocada em uma solução aquosa de ácido clorídrico, havendo a formação do ZnC
2 (aq) + H2 (g): reação que ocorre quando uma lâmina de zinco é colocada em uma solução aquosa de ácido clorídrico, havendo a formação do ZnC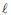 2 (aq) e gás hidrogênio.
2 (aq) e gás hidrogênio.Reação 4:
BaC
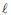 2 (aq) + Na2 SO4 (aq) BaSO4 (s) + 2 NaC(aq): a reação de cloreto de bário com sulfato de sódio produz o cloreto de sódio e o sulfato de bário precipitado.
2 (aq) + Na2 SO4 (aq) BaSO4 (s) + 2 NaC(aq): a reação de cloreto de bário com sulfato de sódio produz o cloreto de sódio e o sulfato de bário precipitado. Após analisar essas reações, uma estudante de Química fez as seguintes afirmações:
I – As reações 1 e 3 são de “síntese”, e a reação 2 é de “decomposição”.
II – As reações 3 e 4 são, respectivamente, de “simples troca” e de “dupla troca”.
III – A reação 2 é de decomposição.
IV – A reação 1 é de síntese.
Com base na teoria das classificações das reações químicas, a estudante fez afirmações corretas APENAS em
Provas
Questão presente nas seguintes provas
O hidrogênio pode ser produzido por eletrólise da água, conforme as reações catódica e anódica indicadas a seguir.
2 H+ + 2 e → H2
H2 O→2 H+ + ½ O2 + 2 e
Considere as seguintes afirmativas:
I – Os potenciais normais de eletrodo são independentes do pH.
II – A diferença de potencial normal da célula é independente do pH.
III – Os sobrepotenciais são independentes da composição da solução.
De acordo com o exposto acima, está correto o que se afirma em
2 H+ + 2 e → H2
H2 O→2 H+ + ½ O2 + 2 e
Considere as seguintes afirmativas:
I – Os potenciais normais de eletrodo são independentes do pH.
II – A diferença de potencial normal da célula é independente do pH.
III – Os sobrepotenciais são independentes da composição da solução.
De acordo com o exposto acima, está correto o que se afirma em
Provas
Questão presente nas seguintes provas
A massa, em gramas, de uma amostra de NaC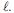 foi medida usando-se cinco balanças analíticas. Devido a problemas com a calibração dessas balanças, os resultados obtidos foram ligeiramente diferentes, como os apresentados abaixo. A medida com o maior número de algarismos significativos é
foi medida usando-se cinco balanças analíticas. Devido a problemas com a calibração dessas balanças, os resultados obtidos foram ligeiramente diferentes, como os apresentados abaixo. A medida com o maior número de algarismos significativos é
 foi medida usando-se cinco balanças analíticas. Devido a problemas com a calibração dessas balanças, os resultados obtidos foram ligeiramente diferentes, como os apresentados abaixo. A medida com o maior número de algarismos significativos é
foi medida usando-se cinco balanças analíticas. Devido a problemas com a calibração dessas balanças, os resultados obtidos foram ligeiramente diferentes, como os apresentados abaixo. A medida com o maior número de algarismos significativos éProvas
Questão presente nas seguintes provas
Sandra pegou uma jarra que continha um litro e meio de suco e encheu dois copos de 300 mL cada. Quantos mililitros de suco sobraram dentro da jarra?
Provas
Questão presente nas seguintes provas
Maria está lendo um livro de 200 páginas. No primeiro dia, ela leu até a página 14. No segundo dia, ela leu as 17 páginas seguintes. Quantas páginas ainda faltam para que Maria termine de ler esse livro?
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container