Foram encontradas 200 questões.
Segundo J. Gimeno Sacristán (2000), “a visão do currículo como algo que se constrói, exige um tipo de intervenção ativa discutida explicitamente num processo de deliberação aberta por parte dos agentes participantes... para que não seja uma mera reprodução de decisões e modelações implícitas.” De acordo com essa concepção, os agentes participantes devem ser:
Provas
Questão presente nas seguintes provas
Se os alunos observarem diariamente o nascer e o pôr do sol, perceberão a regularidade dos pontos de nascente e poente. Ficará fácil a determinação dos pontos cardeais usando a seguinte convenção:
Provas
Questão presente nas seguintes provas
- Química OrgânicaReações OrgânicasReações Orgânicas: Substituição, Adição e Eliminação
- Química OrgânicaReações OrgânicasReações Orgânicas: Oxidação, Redução e Polimerização
Considere a sequência de reações mostrada a seguir:
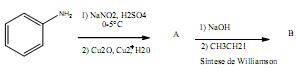
Considere a sequência de reações mostrada a seguir: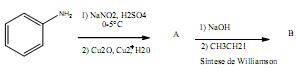
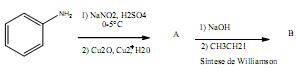
A fórmula estrutural correta do composto B é:
Provas
Questão presente nas seguintes provas
O Modelo Atômico de Bohr foi o primeiro a aplicar o conceito de quantização da energia e contribuiu decisivamente para a compreensão da estrutura atômica. Segundo esse modelo, quando um elétron absorve energia suficiente, é promovido a um estado ou nível eletrônico (n) de maior energia (estado excitado ou ativado). Ao retornar ao estado fundamental, emite ondas eletromagnéticas (radiação). Suponha que o elétron do átomo de hidrogênio, no estado fundamental, absorve energia, sendo promovido para o quarto nível de energia. O comprimento de onda da radiação emitida pelo elétron, ao retornar ao estado fundamental, em nanômetros (nm), é aproximadamente igual a:
Dados:
constante de Rydberg (R)= 2,18.10-18 J,
constante de Planck (h)= 6,67.10-34 J.s, velocidade da luz (c)= 3,00.108 m.s-1
Dados:
constante de Rydberg (R)= 2,18.10-18 J,
constante de Planck (h)= 6,67.10-34 J.s, velocidade da luz (c)= 3,00.108 m.s-1
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
O peróxido de hidrogênio (H2 O2 ) é muito usado em reações de óxido-redução (ou redox), já que pode atuar como agente oxidante ou redutor. É vendido comercialmente na forma de soluções aquosas de diferentes concentrações. Em uma análise para determinar a concentração de uma amostra, 5,10 g de uma água oxigenada comercial foram diluídos com água até 250 mL. Uma alíquota de 25 mL da mesma solução foi titulada por uma solução básica de cloreto de cromo III (CrCl 3 ), conforme a equação não balanceada abaixo:
CrCl 3 (aq) + NaOH (aq) + H2 O 2 (aq) → NaCl (aq) + Na2 CrO 4 (aq) + H2 O (l)
Sabendo que foram gastos 50,00 mL de solução básica de CrCl 3 de concentração 0,01 mol.L-1 , a porcentagem em massa (% m) de peróxido de hidrogênio na amostra de água oxigenada é igual a:
CrCl 3 (aq) + NaOH (aq) + H2 O 2 (aq) → NaCl (aq) + Na2 CrO 4 (aq) + H2 O (l)
Sabendo que foram gastos 50,00 mL de solução básica de CrCl 3 de concentração 0,01 mol.L-1 , a porcentagem em massa (% m) de peróxido de hidrogênio na amostra de água oxigenada é igual a:
Provas
Questão presente nas seguintes provas
A água usada no abastecimento de comunidades humanas requer padrões de qualidade. Assim, ela não deve apresentar sabor, odor e aparência desagradáveis, bem como não deve conter substâncias nocivas e micro-organismos patogênicos. Substâncias orgânicas, como, por exemplo, os compostos 2-trans-6-cis-nonadienal e 3-cis-hexen-1-ol produzidos por algas, em níveis muito baixos (nanograma.L-1 ), causam alterações no sabor e odor.
Em relação à ocorrência de isomeria nos compostos citados, é correto afirmar que:
Em relação à ocorrência de isomeria nos compostos citados, é correto afirmar que:
Provas
Questão presente nas seguintes provas
O Índio e o Tálio são os elementos naturais mais pesados do grupo 13 da classificação periódica. O Alumínio é o elemento mais conhecido e abundante deste grupo, tendo suas propriedades químicas dominadas pelo estado de oxidação +3, ou seja, forma o íon Al 3+. Entretanto, o Índio e o Tálio apresentam frequentemente o estado de oxidação +1. A tendência a formar íons com carga duas unidades menor que a usual para o grupo também é verificada entre os elementos mais pesados dos grupos 14 e 15, sendo conhecida pelo nome de:
Provas
Questão presente nas seguintes provas
Uma amostra de alumínio metálico de massa 21,6 g é completamente dissolvida em solução aquosa de ácido clorídrico e o gás liberado na reação é coletado e colocado em um balão de 25 L, onde a pressão era de 3,0 atm. Em seguida, o gás é aquecido até 127°C. Considerando o gás como ideal, a pressão dentro do balão, em atm, após ser alcançada a temperatura, é aproximadamente igual a:
Dado: massa molar do Al =27g.mol -1
Dado: massa molar do Al =27g.mol -1
Provas
Questão presente nas seguintes provas
- Química OrgânicaFunções Oxigenadas: Cetona, Aldeído, Éter, Éster, Ácido Carboxílico etc.
- Química OrgânicaTipos de Reagentes e Mecanismos das Reações Orgânicas
A reação de aldeídos e cetonas com ilídeos de fósforo, conhecida como Reação de Wittig, conferiu o prêmio Nobel de Química de 1979 ao alemão Georg Wittig, que a realizou em 1954. Desde então, tem sido um método muito usado para a síntese de:
Provas
Questão presente nas seguintes provas
Uma célula galvânica é montada com um eletrodo consistindo de uma lâmina de zinco metálico imersa em solução aquosa 1,0 mol.L-1 de sulfato de zinco. O outro eletrodo é o de hidrogênio, com pressão parcial do gás igual a 1 bar e concentração de íons H3 O+ igual a 0,01 mol.L-1 , a 25°C. A força eletromotriz desta célula, em volts, é aproximadamente igual a:
Dados:
Zn 2+(aq) + 2è → Zn(s) E0 = - 0,76V
Dados:
Zn 2+(aq) + 2è → Zn(s) E0 = - 0,76V
2H+(aq) + 2è → H 2(g)E0 = 0,00V
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container