Foram encontradas 410 questões.
A entalpia padrão de combustão (ΔHC
°) de uma substância
pode ser determinada experimentalmente em um calorímetro de
bomba. Um aparelho desses foi calibrado e sua capacidade calorífi
ca determinada foi de 641J.K-1. Ao se promover a queima de
0,64g de glicose (C6H12O6) no calorímetro, nas condições-padrão, a
temperatura aumentou de 15,6K. Então, pode-se afi rmar que ΔHC
°
da glicose, em kJ.mol-1, é aproximadamente igual a:
Provas
Questão presente nas seguintes provas
O arsênio é um elemento químico muito tóxico que, no estado
de oxidação +3, é letal para os humanos em doses de 140mg ou
mais. É encontrado principalmente nos minerais arsenopirita, realgar
e orpimento, que são sulfetos desse elemento. A reação entre
sulfeto de arsênio III, ácido nítrico e água produz ácido sulfúrico,
ácido arsênico e óxido nítrico gasoso. Após escrever a equação
química completa e balanceada, a soma de todos os menores
coefi cientes estequiométricos inteiros é igual a:
Provas
Questão presente nas seguintes provas
A variação de energia livre de Gibbs (ΔG) é uma medida da
variação total de entropia de um sistema e suas vizinhanças, à
pressão e temperatura constantes e prevê a espontaneidade da
ocorrência de um processo, de acordo com a segunda Lei da Termodinâmica.
Cinco reações químicas, numeradas por I, II, III, IV e
V, cujas variações de entalpia (ΔH) e entropia (ΔS) são conhecidas,
devem ser escolhidas para sua realização à mesma temperatura.
São mostrados a seguir os dados relativos a cada uma das reações:
Reação I - ΔH positivo e ΔS negativo, sendo que o ΔS multiplicado
pela temperatura gera um valor numérico menor que o do ΔH.
Reação II - ΔH positivo e ΔS positivo, sendo que o ΔS multiplicado
pela temperatura gera um valor numérico menor que o de ΔH.
Reação III - ΔH positivo e ΔS negativo, sendo que o ΔS multiplicado
pela temperatura gera um valor numérico maior que o de ΔH.
Reação IV - ΔH negativo e ΔS negativo, sendo que o ΔS multiplicado
pela temperatura gera um valor numérico maior que o de ΔH.
Reação V - ΔH positivo e ΔS positivo, sendo que o ΔS multiplicado
pela temperatura gera um valor numérico maior que o de ΔH.
Segundo dados exclusivamente termodinâmicos, a reação a ser
escolhida é a de número:
Provas
Questão presente nas seguintes provas
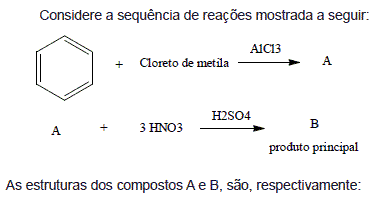
Provas
Questão presente nas seguintes provas
Um químico titula 50,00 mL de uma solução de ácido sulfúrico
com uma solução 0,2500 mol.L-1 de hidróxido de sódio. Entretanto,
ele se distrai e ultrapassa o ponto de equivalência e tem que fazer
uma titulação de retorno com uma solução 0,2000 mol.L-1 de ácido
clorídrico para obter um ponto final apropriado. Se ele adicionou
65,00 mL de hidróxido e gastou 5,000 mL de ácido clorídrico, o
valor encontrado para a concentração do ácido sulfúrico foi, em
mol.L-1, aproximadamente igual a:
Provas
Questão presente nas seguintes provas

Provas
Questão presente nas seguintes provas
- Química OrgânicaFunções Nitrogenadas: Amina, Amida, Nitrila, Isonitrila e Nitro Composto
- Química OrgânicaFunções Oxigenadas: Cetona, Aldeído, Éter, Éster, Ácido Carboxílico etc.
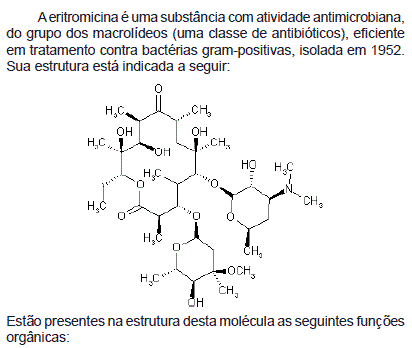
Provas
Questão presente nas seguintes provas

Provas
Questão presente nas seguintes provas
A geometria molecular envolve o estudo da organização
espacial dos átomos em uma molécula e permite a compreensão
de muitas propriedades de uma substância. A “Teoria da Repulsão
dos Pares Eletrônicos da Camada de Valência” (RPECV ou
VSEPR em inglês) é uma ferramenta útil na sua determinação.
De acordo com esta teoria, as formas moleculares corretas das
espécies químicas XeF4, ICl3, TeO3 e POCl3 são,respectivamente:
Provas
Questão presente nas seguintes provas
Considere quatro elementos químicos representados genericamente
por A, B, M e R, de números atômicos consecutivos
e crescentes. Sabe-se que B é o halogênio que demanda mais
energia para formar um cátion. Então, a soma dos números de
elétrons dos íons A2- e R+ é igual a:
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container