Foram encontradas 780 questões.
O ozônio, gás presente na estratosfera terrestre, responsável pela proteção da Terra contra os raios ultravioleta, converte-se em oxigênio, conforme a reação global seguinte.
!$ 2\,O_3(g) \rightharpoonup 3\,O_2(g) !$
Uma proposta de mecanismo para essa reação é dada a seguir.
I. !$ O_3 (g) \rightharpoonup O_2(g) + O(g) !$
II.!$ O_3(g) + O(g) \rightharpoonup 2\,O_2(g) !$
Com base nessas informações, julgue o próximo item.
A lei de velocidade de reações que ocorrem em muitas etapas é determinada pela reação global e, no caso da degradação do ozônio, ela é igual a ν = k [O3]2 [O2]3, em que ν representa a velocidade da reação, k, a constante de velocidade e [O3] e [O2], as concentrações em quantidade de matéria de O3 e O2, respectivamente.
Provas
O ozônio, gás presente na estratosfera terrestre, responsável pela proteção da Terra contra os raios ultravioleta, converte-se em oxigênio, conforme a reação global seguinte.
!$ 2\,O_3(g) \rightharpoonup 3\,O_2(g) !$
Uma proposta de mecanismo para essa reação é dada a seguir.
I. !$ O_3 (g) \rightharpoonup O_2(g) + O(g) !$
II.!$ O_3(g) + O(g) \rightharpoonup 2\,O_2(g) !$
Com base nessas informações, julgue o próximo item.
A espécie O (g) é o catalisador da reação.
Provas
O ozônio, gás presente na estratosfera terrestre, responsável pela proteção da Terra contra os raios ultravioleta, converte-se em oxigênio, conforme a reação global seguinte.
!$ 2\,O_3(g) \rightharpoonup 3\,O_2(g) !$
Uma proposta de mecanismo para essa reação é dada a seguir.
I. !$ O_3 (g) \rightharpoonup O_2(g) + O(g) !$
II.!$ O_3(g) + O(g) \rightharpoonup 2\,O_2(g) !$
Com base nessas informações, julgue o próximo item.
A degradação do ozônio é uma reação de dissociação.
Provas
O ozônio, gás presente na estratosfera terrestre, responsável pela proteção da Terra contra os raios ultravioleta, converte-se em oxigênio, conforme a reação global seguinte.
!$ 2\,O_3(g) \rightharpoonup 3\,O_2(g) !$
Uma proposta de mecanismo para essa reação é dada a seguir.
I. !$ O_3 (g) \rightharpoonup O_2(g) + O(g) !$
II.!$ O_3(g) + O(g) \rightharpoonup 2\,O_2(g) !$
Com base nessas informações, julgue o próximo item.
A reação da etapa II do mecanismo proposto ocorrerá se a energia potencial do complexo ativado for menor que a dos reagentes.
Provas
O ozônio, gás presente na estratosfera terrestre, responsável pela proteção da Terra contra os raios ultravioleta, converte-se em oxigênio, conforme a reação global seguinte.
!$ 2\,O_3(g) \rightharpoonup 3\,O_2(g) !$
Uma proposta de mecanismo para essa reação é dada a seguir.
I. !$ O_3 (g) \rightharpoonup O_2(g) + O(g) !$
II.!$ O_3(g) + O(g) \rightharpoonup 2\,O_2(g) !$
Com base nessas informações, julgue o próximo item.
A etapa II do mecanismo proposto, em que a molécula de ozônio reage com o oxigênio atômico, é bimolecular.
Provas
O ozônio, gás presente na estratosfera terrestre, responsável pela proteção da Terra contra os raios ultravioleta, converte-se em oxigênio, conforme a reação global seguinte.
!$ 2\,O_3(g) \rightharpoonup 3\,O_2(g) !$
Uma proposta de mecanismo para essa reação é dada a seguir.
I. !$ O_3 (g) \rightharpoonup O_2(g) + O(g) !$
II.!$ O_3(g) + O(g) \rightharpoonup 2\,O_2(g) !$
Com base nessas informações, julgue o próximo item.
Se a taxa de produção de oxigênio !$ (d[O_2]/dt) !$ for igual a !$ 3,0 \times 10^{-5} !$ mol/s, a taxa de consumo de ozônio !$ (d[O_3]/dt) !$ será igual a !$ -2,0 \times 10^{-5} !$ mol/s.
Provas
Os resíduos de medicamentos têm-se tornado os poluentes que mais afetam recursos hídricos. Entre eles se destacam os analgésicos. O ácido acetilsalicílico (HAS; M = 180,0 g/mol) é um analgésico cuja concentração em um comprimido pode ser determinada por titulação com NaOH, na presença de fenolftaleína. A proporção de NaOH para HAS na titulação é 1:1. A dipirona sódica, outro analgésico de grande interesse, dado o seu intenso uso pela população, sofre degradação de acordo com a reação representada a seguir.
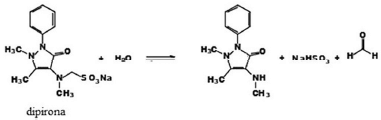
Com base nessas informações, julgue o próximo item.
Nessa reação, a dipirona atua como uma base de Br⌀nsted-Lowry.
Provas
Os resíduos de medicamentos têm-se tornado os poluentes que mais afetam recursos hídricos. Entre eles se destacam os analgésicos. O ácido acetilsalicílico (HAS; M = 180,0 g/mol) é um analgésico cuja concentração em um comprimido pode ser determinada por titulação com NaOH, na presença de fenolftaleína. A proporção de NaOH para HAS na titulação é 1:1. A dipirona sódica, outro analgésico de grande interesse, dado o seu intenso uso pela população, sofre degradação de acordo com a reação representada a seguir.

Com base nessas informações, julgue o próximo item.
A degradação da dipirona ocorre por hidrólise.
Provas
Os resíduos de medicamentos têm-se tornado os poluentes que mais afetam recursos hídricos. Entre eles se destacam os analgésicos. O ácido acetilsalicílico (HAS; M = 180,0 g/mol) é um analgésico cuja concentração em um comprimido pode ser determinada por titulação com NaOH, na presença de fenolftaleína. A proporção de NaOH para HAS na titulação é 1:1. A dipirona sódica, outro analgésico de grande interesse, dado o seu intenso uso pela população, sofre degradação de acordo com a reação representada a seguir.

Com base nessas informações, julgue o próximo item.
O NaOH é um óxido básico binário.
Provas
Os resíduos de medicamentos têm-se tornado os poluentes que mais afetam recursos hídricos. Entre eles se destacam os analgésicos. O ácido acetilsalicílico (HAS; M = 180,0 g/mol) é um analgésico cuja concentração em um comprimido pode ser determinada por titulação com NaOH, na presença de fenolftaleína. A proporção de NaOH para HAS na titulação é 1:1. A dipirona sódica, outro analgésico de grande interesse, dado o seu intenso uso pela população, sofre degradação de acordo com a reação representada a seguir.

Com base nessas informações, julgue o próximo item.
A função da fenolftaleína nessa titulação é tamponar a solução.
Provas
Caderno Container