Foram encontradas 847 questões.
O biodísel, assim chamado por ser um combustível derivado de fontes renováveis vegetais, pode ser produzido por meio de diferentes técnicas, entre as quais se destacam a esterificação, a transesterificação e o craqueamento térmico e(ou) catalítico. Nessas técnicas de produção, são utilizados como matéria-prima óleos e gorduras extraídos de espécies vegetais (nativas ou não) existentes no Brasil, tais como a soja, o dendê, a mamona.
A tabela abaixo resume algumas propriedades físicoquímicas de certos óleos vegetais e de dois tipos de óleo dísel.
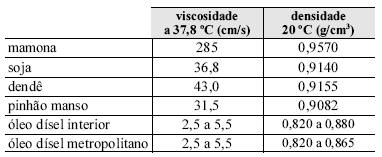
Considerando as informações do texto e os dados da tabela, assinale a opção correta com relação ao biodísel.
Provas
O clorofórmio, CHCl3 , empregado como solvente para produtos naturais, fumigante (para solo), anestésico e droga, é produto altamente tóxico ao organismo humano. Considerando que o valor da densidade desse produto é 1,5 g/mL a 20 ºC, calcule o volume necessário dessa substância para preparar 500 mL de uma solução com concentração em massa correspondente a 12,0 g/L e assinale a opção com a correta indicação desse volume e da vidraria que deve ser utilizada no preparo dessa solução, de forma que o erro percentual associado à medida seja o menor possível.
Provas
As espectrometrias de emissão por plasma, arco e centelha oferecem muitas vantagens em relação às espectrometrias de chama e aos métodos de absorção eletrotérmica. Acerca desse assunto, assinale a opção correta.
Provas
A teoria da ligação de valência (TLV) permite explicar como são associados os ligantes de um metal em um complexo, com base nos orbitais que participam dessas ligações coordenadas, além de fornecer o tipo de hibridação e a geometria do composto. Considerando que Z(H) = 1; Z(N) = 7; Z(F) = 9; Z(CR) = 17; Z(Co) = 27; Z(Ni) = 28; Z(Pt) = 78; assinale a opção que apresenta uma associação correta entre a fórmula do complexo, o tipo de hibridação.
Provas
Ao observar, na prateleira de um supermercado, uma garrafa de 750 mL de um vinho que continha, segundo informações do rótulo, 12,0% em massa de álcool, um consumidor teve a curiosidade de saber o conteúdo calórico nutricional dessa bebida.
Nessa situação, considerando-se que o calor de combustão do etanol, a 25 ºC, é -1.380 kJ/mol, que a densidade do vinho é igual a 0,80 g/mL e que 1 cal = 4,18 J, é correto afirmar que o conteúdo calórico nutricional contido em 750 mL desse vinho é
Provas
Considerando que a faixa de viragem de pH para o vermelho de metila é de 4,4 a 6,2 e, para o vermelho de cresol, de 1,2 a 2,8, assinale a opção que apresenta ação que gera apenas erros indeterminados de análise.
Provas
A equação a seguir representa a oxidação da magnetita (Fe3 O4 ) em hematita (Fe2 O3 ). 2 Fe3 O4 (s) + ½ O2 (g) 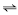 3 Fe2 O3 (s)
3 Fe2 O3 (s) 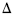 Hº f = -235,8 kJ/mol Considere-se que a reação acima se processe, em equilíbrio, em um sistema fechado à temperatura de 298 K e pressão de 1 atm. Nessa situação, caso o volume do recipiente onde se encontram as substâncias reagentes, sob condições isotérmicas, diminua, é correto afirmar que
Hº f = -235,8 kJ/mol Considere-se que a reação acima se processe, em equilíbrio, em um sistema fechado à temperatura de 298 K e pressão de 1 atm. Nessa situação, caso o volume do recipiente onde se encontram as substâncias reagentes, sob condições isotérmicas, diminua, é correto afirmar que
Provas
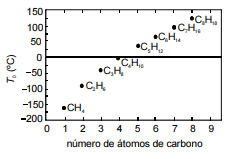
Willian R. Rocha. In: Química Nova na Escola, n.º 4, 2001, p. 31-7.
Considerando a figura acima, que mostra a variação da temperatura de ebulição de vários hidrocarbonetos lineares em função do número de átomos de carbono em suas moléculas, assinale a opção que apresenta uma explicação correta para as diferenças nas temperaturas de ebulição dessas substâncias.
Provas
A sacarose, composta por uma molécula de 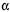 -D-glicose e uma de
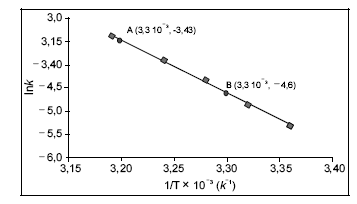
-D-glicose e uma de 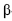 -D-frutose, tendo os átomos de carbono C1 da glicose e C2 da frutose participação na ligação glicosídica, é comumente conhecida como açúcar, sendo extraída para distribuição comercial da cana-de-açúcar (Sacharum officinarum) e da beterraba (Beta vulgaris). No estômago de mamíferos, a sacarose é digerida por hidrólise ácida, que é o mesmo processo usado, em laboratório, para se obterem glicose e frutose. Estas, resultantes da hidrólise da sacarose, são rapidamente absorvidas no intestino delgado, penetrando na corrente sanguínea. Por esses motivos, a sacarose é uma fonte de energia química rápida (com um conteúdo calórico de 17 kJ/g) e causa, logo após sua ingestão, a subida dos níveis sanguíneos de glicose. A partir do gráfico a seguir (ln k × 1/T), em que k representa a constante de velocidade da reação e T, a temperatura absoluta, é possível determinar um dos parâmetros de Arrhenius, isto é, a energia de ativação, Ea , para a hidrólise ácida da sacarose. Considere-se que a velocidade da reação dependa exclusivamente da concentração de sacarose e observe-se que dois pontos da reta são mostrados no gráfico.
-D-frutose, tendo os átomos de carbono C1 da glicose e C2 da frutose participação na ligação glicosídica, é comumente conhecida como açúcar, sendo extraída para distribuição comercial da cana-de-açúcar (Sacharum officinarum) e da beterraba (Beta vulgaris). No estômago de mamíferos, a sacarose é digerida por hidrólise ácida, que é o mesmo processo usado, em laboratório, para se obterem glicose e frutose. Estas, resultantes da hidrólise da sacarose, são rapidamente absorvidas no intestino delgado, penetrando na corrente sanguínea. Por esses motivos, a sacarose é uma fonte de energia química rápida (com um conteúdo calórico de 17 kJ/g) e causa, logo após sua ingestão, a subida dos níveis sanguíneos de glicose. A partir do gráfico a seguir (ln k × 1/T), em que k representa a constante de velocidade da reação e T, a temperatura absoluta, é possível determinar um dos parâmetros de Arrhenius, isto é, a energia de ativação, Ea , para a hidrólise ácida da sacarose. Considere-se que a velocidade da reação dependa exclusivamente da concentração de sacarose e observe-se que dois pontos da reta são mostrados no gráfico.
Considerando-se que a constante universal dos gases vale 8,3145 J·K-1· mol-1 , é correto concluir que o valor da energia de ativação da hidrólise ácida da sacarose é
Provas
No método de titulação, a solução cuja concentração é conhecida, chama-se solução-padrão. Para que uma substância seja considerada um padrão primário, ela deve atender a alguns requisitos necessários e outros desejáveis. É condição sine qua non, por exemplo, que a substância tenha alta pureza. Entre as condições desejáveis, está a de que ela deve ter elevada massa molar. Assinale a opção em se justifica a necessidade de o padrão primário atender a esse critério desejável.
Provas
Caderno Container