Foram encontradas 50 questões.
A figura a seguir que deve ser utilizada para responder as questões 32, 33 e 34, apresenta um esquema para uma pilha galvânica.
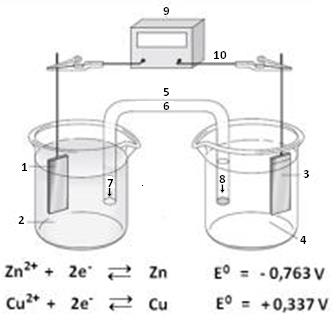
Os números 1 e 3 indicam, respectivamente,
Provas
- Química CinéticaRepresentação das Transformações Químicas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
- Sistemas de EquilíbrioSistemas Homogêneos: Equilíbrio Químico na Água
Sobre uma titulação complexométrica com EDTA, é correto afirmar:
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
- Técnicas de Laboratório
Sobre as análises volumétricas afirma-se:
I Para a determinação da quantidade do material analisado em uma análise volumétrica considera-se, como ponto final da titulação, o ponto estequiométrico da titulação.
II Deve-se levar em conta a estequiometria da reação, ou seja, os coeficientes estequiométricos para a reação entre o indicador e o analito.
III O volume gasto na titulação deve ser utilizado como parâmetro de comparação para a determinação do analito.
IV Para a determinação da quantidade de um ácido fraco, considera-se como ponto final da titulação o ponto em que o meio reacional apresenta o equilíbrio de ionização desse ácido.
Dentre as afirmativas, estão corretas apenas
Provas
Em relação às análises gravimétricas, considere as afirmativas a seguir.
I Na determinação da matéria etérea, é comum utilizar-se o método conhecido como soxhlet, em que a amostra sofre extração utilizando solvente não aquoso e o resíduo é pesado após evaporação do solvente.
II Na determinação de umidade em uma amostra, o teor de água é calculado após aquecimento da amostra até que se obtenha as cinzas.
III Na determinação do teor de ferro em um minério por gravimetria é necessária a abertura da amostra utilizando solução ácida, seguida de precipitação utilizando hidróxido de amônio e aquecimento a 900 ºC.
IV A gravimetria é uma técnica analítica para determinação quantitativa de compostos em matrizes diversas, desde que sejam de origem mineral.
Dentre as afirmativas, estão corretas apenas
Provas
Para análise de um analito de natureza orgânica e insolúvel em água, em amostras de solo, os métodos de preparação de amostras utilizados são
Provas
Sobre métodos de amostragem, considere as afirmativas a seguir.
I Amostragem é o processo pelo qual a coleta de amostras é executado, considerando-se como partes desse processo as etapas de aquisição, acondicionamento, transporte e conservação até o momento de sua preparação para análise.
II A escolha de um método de preparação de amostra depende do estado físico da amostra, de sua natureza química, de sua composição e da possibilidade de eliminação de interferentes.
III Contra-prova diz respeito a um tipo de amostra que se mantém em condições ótimas de conservação e que se mantém sob a guarda do laboratório até que seja utilizada para a necessidade de repetições.
IV Dentre os diversos tipos de métodos de amostragem, pode-se citar o quarteamento que pode ser aplicado para amostras sólidas, como por exemplo, para amostragem de solos.
Dentre as afirmativas, estão corretas
Provas
O ácido acético é considerado um ácido fraco, cuja constante de equilíbrio equivale a 1,75 x 10-5. Isso significa que uma solução aquosa 0,10 mol/L desse ácido apresenta no equilíbrio
Provas
- Química CinéticaRepresentação das Transformações Químicas
- Sistemas de EquilíbrioSistemas Homogêneos: Equilíbrio Químico na Água
A massa, em gramas, de HCl contida em um litro de uma solução desse ácido com pH = 2 é
Provas
Foi solicitado a um técnico que preparasse 1,0 L de uma solução 100 ppm do íon cloreto. No laboratório, o técnico encontrou um frasco que continha a substância cloreto de cálcio (CaCl2.2H2O). A massa desse sal, em gramas, que deve ser pesada pelo técnico para que obtenha a solução é
Provas
O sulfato ferroso (FeSO4) é usado em medicamentos contra anemia e, normalmente, apresenta uma quantidade de 68 mg dessa substância para cada 1,0 mL da amostra. O valor da concentração dessa solução em mol/L corresponde a
Provas
Caderno Container