Foram encontradas 60 questões.
Analise as reações abaixo.
I. SO2 + H2O2 -› H2SO4
II. SO2 + H2O -› H2SO3
III. SO2 + NH4OH -› NH4HSO3
Das reações, ocorre o fenômeno de oxirredução em
Provas
Questão presente nas seguintes provas
Considerando o sistema tampão formado pelo par ácido/base conjugada ácido
propanoico/íon propanoato (CH3CH2COOH/CH3CH2COO-), calcule o valor de pH de 1,0 L de solução cuja
concentração de ácido propanoico é 0,0300 mol L-1
e de propanoato de sódio é 0,300 mol L-1
. A resposta
CORRETA é: (Ka = 1,0 x 10-5
)
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Em um laboratório de análises químicas, solicitou-se ao técnico o preparo e a padronização
de soluções de hidróxido de sódio (NaOH) e ácido clorídrico (HCl), ambas na concentração de 0,1 mol L-1
.
Dessa forma, o técnico procedeu a pesagem da massa de NaOH calculado em um béquer e dissolveu em
água destilada, agitando com o auxílio de um bastão de vidro. Transferiu a solução para um balão
volumétrico e completou-o com água até a marca da aferição. Posteriormente, mediu um volume adequado
de solução concentrada de ácido clorídrico e transferiu para um balão volumétrico preenchido parcialmente
com água destilada, completando o volume com água até a marca da aferição. A padronização da solução
de NaOH foi feita por titulometria, utilizando biftalato de potássio como padrão. Em seguida, o técnico
utilizou essa solução padronizada para descobrir a concentração verdadeira da solução de HCl, também por
titulometria. Analisando esse procedimento, é CORRETO afirmar:
Provas
Questão presente nas seguintes provas
- Química CinéticaRepresentação das Transformações Químicas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Uma amostra de 6,000 g de hematita, um mineral de ferro, foi dissolvida completamente em
ácido, e o ferro presente foi totalmente reduzido a Fe2+. A seguir, a amostra dissolvida foi transferida para
um balão volumétrico de 250,0 mL, o qual foi completado com água destilada até a marca de aferição. Uma
alíquota de 10,00 mL dessa solução contendo o Fe2+ foi titulada com exatamente 25,00 mL de uma solução
padrão 0,020 mol L-1
de dicromato, em meio ácido, segundo a equação abaixo.
Cr2O72-(aq) + 6Fe2+(aq) + 14H+(aq) -› 2Cr3+(aq) + 6Fe3+(aq) + 7H2O(l)
Considerando a estequiometria dessa reação, a porcentagem em massa de Fe na amostra analisada é, aproximadamente, igual a
Cr2O72-(aq) + 6Fe2+(aq) + 14H+(aq) -› 2Cr3+(aq) + 6Fe3+(aq) + 7H2O(l)
Considerando a estequiometria dessa reação, a porcentagem em massa de Fe na amostra analisada é, aproximadamente, igual a
Provas
Questão presente nas seguintes provas
O fenômeno de corrosão metálica causa grandes prejuízos às indústrias, pois nesse
processo ocorre a dissolução lenta da superfície de equipamentos, quando os mesmos são expostos ao ar,
em contato com o solo ou água do mar. Com o objetivo de minimizar a corrosão do ferro em equipamentos,
são utilizados os chamados “eletrodos de sacrifício”, os quais são formados por barras de outros metais,
convenientemente escolhidos que, quando colocados em contato com a superfície do equipamento, sofrem
corrosão no lugar do ferro.

Com base nos dados tabelados, são considerados “eletrodos de sacrifício” adequados as barras de

Com base nos dados tabelados, são considerados “eletrodos de sacrifício” adequados as barras de
Provas
Questão presente nas seguintes provas
A célula eletroquímica representada pelo esquema da figura que segue, onde V é um
voltímetro e S é uma ponte salina que contém uma solução saturada de nitrato de potássio (KNO3), possui
um eletrodo de zinco imerso em uma solução de nitrato de zinco, Zn(NO3)2, e outro eletrodo de prata imerso
em uma solução de nitrato de prata, AgNO3, nas concentrações indicadas a 25ºC.
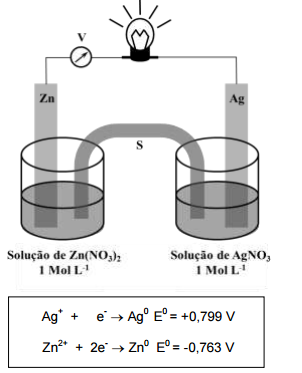
Considerando a célula eletroquímica e os potenciais-padrão de redução acima representados, é CORRETO afirmar:

Considerando a célula eletroquímica e os potenciais-padrão de redução acima representados, é CORRETO afirmar:
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSubstâncias Inorgânicas: dissociação iônica e ionização, conceitos de ácido-base
A tabela abaixo mostra os valores de constantes de dissociação, Kb, a 25 °C, para
diversas bases. 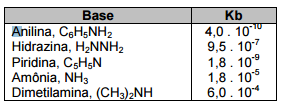
Analisando esses valores, é CORRETO afirmar:

Analisando esses valores, é CORRETO afirmar:
Provas
Questão presente nas seguintes provas
A quantidade de carbono em um composto orgânico foi determinada através da queima de
0,2121 g do composto em um fluxo de oxigênio. O CO2 produzido na reação foi coletado em uma solução
de hidróxido de bário. Se 0,6000 g de BaCO3 foi formado, a porcentagem de carbono na amostra é
Provas
Questão presente nas seguintes provas
- Química CinéticaRepresentação das Transformações Químicas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
O Cr de uma superfície cromada de dimensões 3,00 x 5,00 cm foi dissolvido em ácido
clorídrico. O pH da solução foi ajustado e, posteriormente, foram adicionados 15,00 mL de solução padrão
de EDTA 0,200 mol L-1
. O reagente em excesso foi retrotitulado com um volume de 4,00 mL de solução
padrão de Cu2+ 0,100 mol L-1
. A massa aproximada, em mg, de Cr em cada centímetro quadrado da
superfície foi
Provas
Questão presente nas seguintes provas
A técnica de cromatografia é utilizada para separação, identificação e quantificação de
componentes químicos em misturas complexas. Essa técnica se baseia na distribuição de substâncias entre
duas fases químicas ou físicas, sendo uma fase estacionária e a outra fase móvel ao longo do sistema.
Com relação aos diferentes tipos de técnicas cromatográficas, é INCORRETO afirmar:
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container