Foram encontradas 50 questões.
Na figura abaixo, aparece uma montagem para filtração.
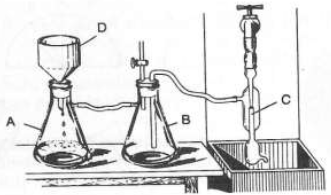
Os materiais A, B, C e D são, respectivamente:
Provas
Considere as soluções abaixo:
I. 0,1 mol L-1 NaCH3COO + 0,1 mol L-1 HCH3COO
II. 0,2 mol L-1 NH3 + 0,1 mol L-1 HCl
III. 0,1 mol L-1 NaCl + 0,1 mol L-1 HCl
IV. 0,1 mol L-1 NaOH + 0,1 mol L-1 HCH3COO
V. 0,2 mol L-1 HCH3COO + 0,1 mol L-1 NaOH
São soluções-tampão:
Provas
Uma solução de sacarose foi preparada pela dissolução de 0,0684 kg de C12H22O11 em uma quantidade de água suficiente para se obter exatamente 0,1000 L de solução, cuja densidade foi de 1,284 kg L-1.
A molalidade da solução de sacarose é:
Provas
Uma amostra de uma liga Al-Mg-Cu, pesando 6,74 g, foi tratada primeiramente com solução de NaOH para dissolver o alumínio. Depois, foi adicionado HCl diluído para dissolver o magnésio, sobrando um resíduo de cobre. A massa resultante após o tratamento alcalino foi de 1,84 g e o resíduo resultante do tratamento ácido pesou 0,540 g.
A composição da liga é:
Provas
Uma solução aquosa de hidróxido de bário foi utilizada para medir a quantidade de gás carbônico produzida de uma reação de oxidação. O gás era forçado a borbulhar na solução e era formado um precipitado. Após o término da reação, o precipitado foi secado e pesado, obtendo-se 986,5 mg.
A massa em gramas, de gás carbônico produzida na reação de oxidação, foi de:
Provas
O volume, em mL, de ácido sulfúrico, com 98,0 % em massa e densidade de 1,86 g mL-1, necessário para preparar 1,00 L de uma solução 2,00 mol L-1 é de:
Provas
Em um balão volumétrico de 100,0 mL colocaram-se 3,812 g de MgCl2. O volume foi completado com água destilada até a marca.
Considerando-se que todo o MgCl2 foi dissolvido, a concentração de íons Cl- na solução, em mol L-1, é de:
Provas
Um ácido HA, com concentração de 5,0 X 10-3 mol dm-3, possui Ka = 5,8 x 10-13 mol dm-3. Sendo a constante de auto-ionização da água KW = 1,0 X 10-14 mol2 dm-6, a equação que deve ser utilizada para o cálculo do pH é
Provas
As seguintes afirmações foram feitas sobre misturas de soluções ácidas e básicas:
I. A mistura de quantidades equimolares de uma solução de base fraca com uma solução de ácido fraco produz sempre uma solução de pH neutro.
II. A mistura de uma quantidade em excesso molar de uma solução de base fraca com uma solução de ácido forte produz uma solução de pH básico.
III. A mistura de uma quantidade em excesso molar de uma solução de base forte com uma solução de ácido fraco produz uma solução tampão de pH básico.
IV. A mistura de uma quantidade em excesso molar de uma solução de ácido fraco com uma solução de base forte produz uma solução tampão de pH ácido.
V. A mistura de quantidades equimolares de uma solução de base fraca com uma solução de ácido forte produz uma solução de pH ácido.
Estão corretas as afirmações:
Provas
Deseja-se preparar 100 mL de uma solução de NaOH 1,0% (m/v) a partir de uma solução “mãe” de NaOH 2,0 mol L-1.
O volume que deve ser retirado da solução-mãe é:
Provas
Caderno Container