Foram encontradas 50 questões.
A autoionização da água é um processo muito importante, pois dependendo da sua posição de equilíbrio
químico, define-se a acidez (ou alcalinidade) das soluções aquosas. Através de experimentos de condutividade
elétrica da água pura e da sua condutância específica, é possível determinar o grau de ionização da água e,
posteriormente, a constante de equilíbrio, Kw, da reação de autoionização. A 25 °C, o valor de Kw é 1,00 x 10-14
.
Por outro lado, para a água pura, a 37 °C, o grau de ionização é 73% maior, tendo em vista que a autoionização
da água é endotérmica. Vale ressaltar que nesta variação de temperatura a concentração molar da água é
praticamente invariável.
Diante das informações e a partir dos seus conhecimentos, assinale a opção que mostra aproximadamente O VALOR DO pOH de uma solução de pH 8,50, a 37 °C:
Dados: densidade da água = 1000 g/L; massa molar da água = 18 g/mol; log(1,73) = 0,24; log(3) = 0,48.
Diante das informações e a partir dos seus conhecimentos, assinale a opção que mostra aproximadamente O VALOR DO pOH de uma solução de pH 8,50, a 37 °C:
Dados: densidade da água = 1000 g/L; massa molar da água = 18 g/mol; log(1,73) = 0,24; log(3) = 0,48.
Provas
Questão presente nas seguintes provas
Num laboratório de Química, para preparar uma solução de ácido sulfúrico é importante seguir algumas
precauções de segurança. Num desses preparos, um técnico dispunha de um banho de gelo e outros materiais,
mostrados na Figura abaixo. O rótulo do produto (ácido sulfúrico concentrado) também é reproduzido
parcialmente, com algumas informações importantes.
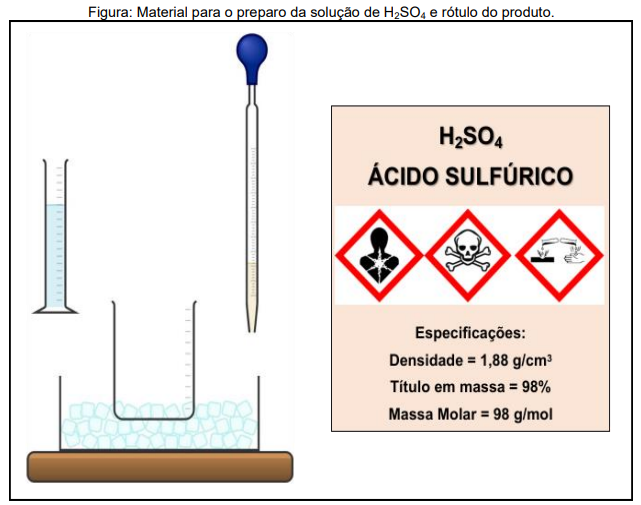
A respeito da preparação da solução de ácido sulfúrico e dos elementos na Figura acima, assinale a opção INCORRETA: Dado: considere a densidade da água = 1 g/mL.

A respeito da preparação da solução de ácido sulfúrico e dos elementos na Figura acima, assinale a opção INCORRETA: Dado: considere a densidade da água = 1 g/mL.
Provas
Questão presente nas seguintes provas
Um certo ácido orgânico, Y, encontra-se parcialmente na forma de dímeros (reação: 2Y(g) ⇌ Y2(g) ), quando em
fase de vapor. Na temperatura de 298 K e sob pressão total de 0,200 atm, este ácido tem um grau de
dimerização de 90%.
Diante dessas informações, assinale a opção que mostra O VALOR DA CONSTANTE DE EQUILÍBRIO, Kp, para a reação de dimerização e a afirmação CORRETA que expressa a influência da pressão (FAVORECE OU DESFAVORECE) na dimerização:
Diante dessas informações, assinale a opção que mostra O VALOR DA CONSTANTE DE EQUILÍBRIO, Kp, para a reação de dimerização e a afirmação CORRETA que expressa a influência da pressão (FAVORECE OU DESFAVORECE) na dimerização:
Provas
Questão presente nas seguintes provas
Em cinética química, os fenômenos que se baseiam num mecanismo de primeira ordem são bastante comuns.
Neste “tipo de cinética”, a quantidade (ou concentração) da espécie reagente diminui exponencialmente ao longo
do tempo. Esse comportamento pode ser visualizado por meio de gráficos que relacionam a concentração do
reagente ou a velocidade do seu consumo com o tempo. A Figura abaixo mostra exemplos destes gráficos
obtidos num experimento com uma reação de primeira ordem. Vale ressaltar que devido à maior simplicidade
matemática de modelos lineares, em geral, para descrever a cinética de primeira ordem, gráficos do logaritmo
natural (ln) da concentração versus tempo são preferidos, fornecendo diretamente a constante de velocidade
através da inclinação da reta.
Figura: Dados cinéticos para uma reação de primeira ordem. Concentração versus tempo e velocidade versus tempo.
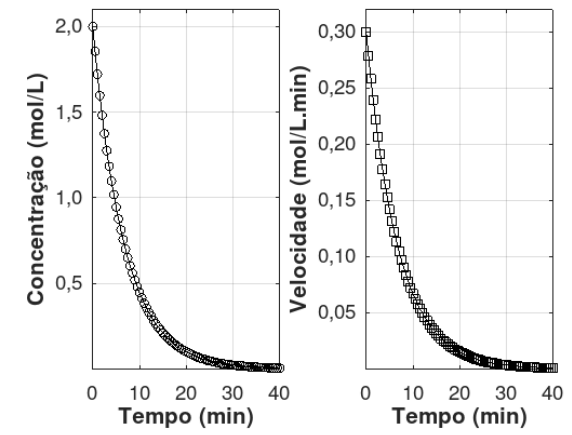
A partir da interpretação dos gráficos mostrados acima, assinale a opção que mostra corretamente O VALOR DO TEMPO DE MEIA-VIDA do processo, em minutos, com precisão de duas casas decimais: Dado: considere ln(2) = 0,693.
Figura: Dados cinéticos para uma reação de primeira ordem. Concentração versus tempo e velocidade versus tempo.

A partir da interpretação dos gráficos mostrados acima, assinale a opção que mostra corretamente O VALOR DO TEMPO DE MEIA-VIDA do processo, em minutos, com precisão de duas casas decimais: Dado: considere ln(2) = 0,693.
Provas
Questão presente nas seguintes provas
A condensação aldólica é uma reação química que ocorre entre um íon enolato e um composto carbonílico,
resultando na formação de um composto β-hidroxi-carbonílico, também conhecido como aldol. Para que haja a
formação do enolato, é utilizada uma base forte que retira um próton do carbono em posição α (alfa) em relação
à carbonila de um aldeído ou de uma cetona. Esse íon enolato atua como nucleófilo e ataca o carbono
carbonílico de outra molécula formando uma ligação carbono-carbono. A condensação aldólica é amplamente
utilizada na síntese de compostos orgânicos, especialmente em sínteses de produtos naturais, medicamentos e
polímeros.
No contexto exposto acima, assinale a ÚNICA opção que contém o nome de um composto carbonílico que NÃO gera o íon enolato na presença de uma base forte:
No contexto exposto acima, assinale a ÚNICA opção que contém o nome de um composto carbonílico que NÃO gera o íon enolato na presença de uma base forte:
Provas
Questão presente nas seguintes provas
Num laboratório de Química, a técnica de refluxo é geralmente usada quando se deseja realizar uma reação
química, em meio líquido, que requer a manutenção de uma temperatura constante durante um longo período de
tempo. O refluxo é usado para permitir que a reação ocorra na temperatura de ebulição do líquido, sem a perda
excessiva de solvente ou de produtos voláteis. Abaixo é apresentado um aparato típico para a realização da
técnica de refluxo:
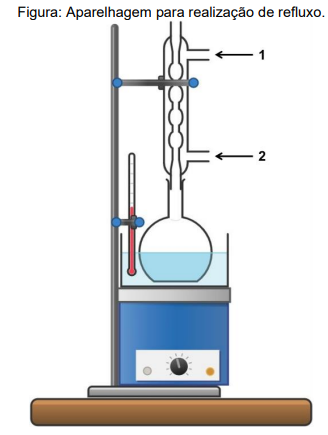
Sobre a técnica citada acima, sua aparelhagem mostrada e demais aspectos relacionados, assinale a opção CORRETA:

Sobre a técnica citada acima, sua aparelhagem mostrada e demais aspectos relacionados, assinale a opção CORRETA:
Provas
Questão presente nas seguintes provas
Atualmente, é comum a comercialização da chamada “água potável alcalina”, cuja publicidade costuma ser feita
com a exaltação dos seus supostos benefícios para a saúde humana. As mensagens comerciais induzem à ideia
de que o produto favorece a redução da acidez no corpo, melhora a digestão e previne certas doenças. Neste
contexto, no ano de 2018, houve uma decisão judicial contra uma marca de água devido à “veiculação de
publicidade enganosa e prática de concorrência desleal”, pois não há evidências científicas confirmando nenhum
dos benefícios, sendo que a própria marca afirmou “que se trata de uma questão ainda em discussão dentro do
meio científico”.
Fonte: https://www.uol.com.br/vivabem/noticias/redacao/2018/11/30/propaganda-de-agua-alcalina-evetada-esse-produto-tem-beneficios.htm. Acesso em 02 de abril de 2023.
Em um desses produtos apresentam-se no rótulo as informações: Classificação - água mineral alcalinobicarbonatada, fluoretada e hipotermal na fonte, pH 8,16 a 25°C. Composição Química (mg/L) - Bicarbonato = 321,20; Sódio = 115,630; Cálcio = 9,692; Sulfeto = 9,31; Cloreto = 9,29; Magnésio = 2,161; Potássio = 0,972; Bário = 0,335; Estrôncio = 0,318; Fluoreto = 0,02.
Sobre as informações acima e a partir dos seus conhecimentos, assinale a opção CORRETA:
(Dados - Massas molares (g/mol): H = 1; C =12; O = 16; Na = 23; Ca = 40; S = 32; Cl = 35,5; Mg = 24; K = 39; Ba = 137; F = 19; Sr = 87,6).
Fonte: https://www.uol.com.br/vivabem/noticias/redacao/2018/11/30/propaganda-de-agua-alcalina-evetada-esse-produto-tem-beneficios.htm. Acesso em 02 de abril de 2023.
Em um desses produtos apresentam-se no rótulo as informações: Classificação - água mineral alcalinobicarbonatada, fluoretada e hipotermal na fonte, pH 8,16 a 25°C. Composição Química (mg/L) - Bicarbonato = 321,20; Sódio = 115,630; Cálcio = 9,692; Sulfeto = 9,31; Cloreto = 9,29; Magnésio = 2,161; Potássio = 0,972; Bário = 0,335; Estrôncio = 0,318; Fluoreto = 0,02.
Sobre as informações acima e a partir dos seus conhecimentos, assinale a opção CORRETA:
(Dados - Massas molares (g/mol): H = 1; C =12; O = 16; Na = 23; Ca = 40; S = 32; Cl = 35,5; Mg = 24; K = 39; Ba = 137; F = 19; Sr = 87,6).
Provas
Questão presente nas seguintes provas
O ácido hialurônico (AH) é uma macromolécula de origem natural, presente em diversos tecidos do corpo
humano, principalmente na pele, cartilagens, líquido sinovial e humor vítreo do olho. É um glicosaminoglicano
composto por unidades repetidas do dissacarídeo formado pela N-acetilglicosamina e o ácido D-glicurônico
(Figura abaixo).

O AH é altamente hidrofílico e capaz de reter grandes quantidades de água, o que lhe confere propriedades viscoelásticas e lubrificantes. Na pele, por exemplo, ele é responsável por manter a hidratação e elasticidade, além de ajudar a preencher o meio extracelular, o que contribui para a uniformidade da superfície cutânea.
Sobre a química do AH e a partir dos seus conhecimentos, assinale a opção CORRETA:

O AH é altamente hidrofílico e capaz de reter grandes quantidades de água, o que lhe confere propriedades viscoelásticas e lubrificantes. Na pele, por exemplo, ele é responsável por manter a hidratação e elasticidade, além de ajudar a preencher o meio extracelular, o que contribui para a uniformidade da superfície cutânea.
Sobre a química do AH e a partir dos seus conhecimentos, assinale a opção CORRETA:
Provas
Questão presente nas seguintes provas
O hidróxido de zinco, Zn(OH)2, por ser um importante precursor do óxido de zinco, ZnO, tem diversas aplicações
em diferentes áreas. Algumas das principais incluem a produção de cosméticos e protetores solares e a
vulcanização da borracha. Esse hidróxido é insolúvel em água, com constante produto de solubilidade, Kps, igual
a 1,2 x 10-17
, a 25 °C.
Diante das informações, assinale a opção que mostra o valor do pH (após o equilíbrio) de uma solução em que são adicionados 0,01 mol/L de Zn2+ e 0,02 mol/L de OH- , a 25 °C: Dados eventualmente necessários: Kw (H2O), a 25 °C = 1,00 x 10-14; (3)1/3 = 1,44; log (1,44) = 0,16; log (2,88) = 0,46; (6)1/2 = 2,45; log (2,45) = 0,39; log (4,9) = 0,69.
Diante das informações, assinale a opção que mostra o valor do pH (após o equilíbrio) de uma solução em que são adicionados 0,01 mol/L de Zn2+ e 0,02 mol/L de OH- , a 25 °C: Dados eventualmente necessários: Kw (H2O), a 25 °C = 1,00 x 10-14; (3)1/3 = 1,44; log (1,44) = 0,16; log (2,88) = 0,46; (6)1/2 = 2,45; log (2,45) = 0,39; log (4,9) = 0,69.
Provas
Questão presente nas seguintes provas
O termo “superácido” é usado para descrever os ácidos mais fortes do que o ácido sulfúrico, um dos ácidos
comuns mais fortes. George Andrew Olah (1927 - 2017), um químico húngaro-estadunidense, ganhou o Prêmio
Nobel de Química em 1994, com a aplicação de superácidos ao estudo de carbocátions. A água é um solvente
incapaz de distinguir os superácidos do ácido sulfúrico, uma vez que ela apresenta o chamado “efeito nivelador”.
Portanto, na quantificação da acidez dos superácidos é comum o uso da função de acidez de Hammett, H0, que
é definida matematicamente como:
H0 = pKa(BH+) - log [BH+] / [B]
onde B é um indicador básico, BH+ é o ácido conjugado desse indicador e pKa(BH+) é a constante de acidez deste último. Quando o indicador é nitroanilina (C6H6N2O2), experimentos realizados para ácidos puros nas mesmas condições, permitem construir a tabela abaixo:
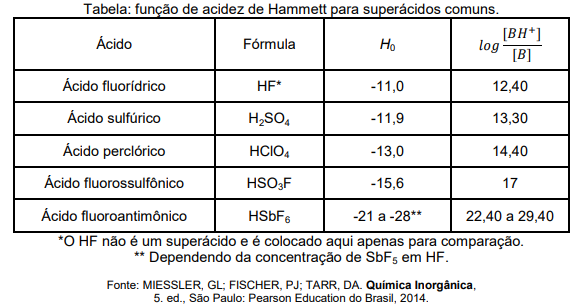
Diante dessas informações, assinale a opção que mostra a ÚNICA reação termodinamicamente espontânea entre pares das substâncias citadas acima:
H0 = pKa(BH+) - log [BH+] / [B]
onde B é um indicador básico, BH+ é o ácido conjugado desse indicador e pKa(BH+) é a constante de acidez deste último. Quando o indicador é nitroanilina (C6H6N2O2), experimentos realizados para ácidos puros nas mesmas condições, permitem construir a tabela abaixo:

Diante dessas informações, assinale a opção que mostra a ÚNICA reação termodinamicamente espontânea entre pares das substâncias citadas acima:
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container