Foram encontradas 50 questões.
Um estudante de química realiza a seguinte reação em equilíbrio.
N2 (g) + 3H2 (g) 2NH3 (g) ΔH = -92 kJ/mol
Considerando o Princípio de Le Chatelier, a alteração que aumentará a concentração de amônia (NH₃) no equilíbrio é:
N2 (g) + 3H2 (g) 2NH3 (g) ΔH = -92 kJ/mol
Considerando o Princípio de Le Chatelier, a alteração que aumentará a concentração de amônia (NH₃) no equilíbrio é:
Provas
Questão presente nas seguintes provas
Em laboratório de síntese de corantes, um composto de fórmula CH3–C6H4–Cl é analisado. Se o grupo metil está na posição 1, e o cloro, na posição 4, o nome do composto é:
Provas
Questão presente nas seguintes provas
Um laboratório químico está acompanhando o progresso da síntese de um fármaco. Para isso, o analista realiza uma cromatografia em camada delgada (CCD), utilizando uma placa de sílica como fase estacionária e uma mistura de solventes orgânicos como fase móvel. Os pontos correspondentes aos reagentes e ao produto são visualizados com um revelador adequado. Durante a análise, o analista observa que alguns compostos migraram mais rapidamente que outros na placa. Essa diferença na migração dos compostos deve-se, principalmente, à(ao):
Provas
Questão presente nas seguintes provas
Uma indústria de suplementos realiza o controle de qualidade de uma solução de ácido ascórbico (vitamina C) por titulação ácido-base. Uma alíquota de 25,0 mL da solução foi titulada com NaOH 0,020 mol/L usando fenolftaleína como indicador. O volume de NaOH gasto para atingir o ponto fi nal foi de 30,0 mL. A reação C6H8O6 + NaOH → C6H7O6Na + H2O é uma neutralização 1:1.
A partir disso, pode-se assumir que a concentração do ácido ascórbico (C6H8O6) na solução, em mol/L, é:
A partir disso, pode-se assumir que a concentração do ácido ascórbico (C6H8O6) na solução, em mol/L, é:
Provas
Questão presente nas seguintes provas
A tabela periódica apresenta tendências de propriedades periódicas. No que se refere à eletronegatividade, na tabela periódica, observa-se que o(a):
Provas
Questão presente nas seguintes provas
Em um laboratório de análise química, um estudante prepara uma solução de um composto orgânico aromático e realiza uma leitura espectrofotométrica no ultravioleta (UV). Ele observa um pico de absorção em ≈ 260 nm. Com base nessa observação, o estudante conclui que o(a):
Provas
Questão presente nas seguintes provas
A estrutura geral de um aminoácido pode ser representada pela seguinte estrutura.
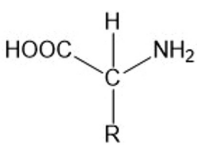
Observa-se que o carbono central está ligado a um grupo amino (–NH2), a um grupo carboxila (–COOH), a um átomo de hidrogênio e a uma cadeia lateral variável (R). Com base nessa estrutura, o caráter anfótero dos aminoácidos decorre do fato de que essas moléculas:

Observa-se que o carbono central está ligado a um grupo amino (–NH2), a um grupo carboxila (–COOH), a um átomo de hidrogênio e a uma cadeia lateral variável (R). Com base nessa estrutura, o caráter anfótero dos aminoácidos decorre do fato de que essas moléculas:
Provas
Questão presente nas seguintes provas
Uma amostra de gás ideal sofre uma transformação isobárica. Se a temperatura absoluta for duplicada, o volume do gás:
Provas
Questão presente nas seguintes provas
A finalidade do Teste de Baeyer é:
Provas
Questão presente nas seguintes provas
Em um laboratório de Química, um estudante realizou dois procedimentos distintos. No primeiro, ao misturar duas substâncias, observou-se aumento da temperatura do recipiente, mesmo sem aquecimento externo. No segundo procedimento, foi necessário fornecer calor ao sistema para que a transformação ocorresse. Com base nessas observações, os processos descritos são classificados, respectivamente, como:
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container