Foram encontradas 64 questões.
A produção de ferro metálico para solda pode ser realizada a partir da reação entre alumínio metálico e óxido férrico, de acordo com a reação abaixo:
![]()
Considerando que essa reação tem um rendimento de 90%, calcule a massa de alumínio necessária para a produção de 11,2 kg de ferro para solda.
Massas molares (g/mol): O = 16; Al = 27; Fe = 56.
Provas
Uma indústria química é especializada na produção de sais de cromato (CrO4 2- ). Uma das reações envolvidas no processo é mostrada abaixo:
![]()
A reação não está balanceada. Faça o balanceamento, considerando os menores inteiros como coeficientes reacionais. A soma desses coeficientes é igual a:
Provas
- Química CinéticaRepresentação das Transformações Químicas
- Química InorgânicaReações InorgânicasCálculo Estequiométrico
O elemento mercúrio é o único metal líquido à temperatura ambiente. Considere uma amostra de 400mL de mercúrio. Quantos átomos do metal, aproximadamente, estão presentes nessa amostra?
Dados: densidade Hg(l) = 13,6 kg/dm3 ; massa molar Hg = 200 g/mol; considere o número de Avogadro = 6 x 1023
Provas
Quando a temperatura é 227ºC, a reação entre os gases PCl3 e Cl2, que forma o produto também gasoso PCl5, tem sua constante de equilíbrio expressa em termos de concentrações molares igual a 3400.
![]()
Considere que a reação acima está em equilíbrio e que as concentrações de PCl3 e Cl2 são 1,0 x 10-3 molL-1 e 1,0 x 10-2 molL-1 , respectivamente. Nessas condições, a pressão de PCl5 no equilíbrio será:
Provas
Uma amostra de água contém íons chumbo (Pb2+) dissolvidos com a concentração igual a 1,0 x 10-4 molL-1 . Para realizar a precipitação desses cátions, adiciona-se progressivamente NaCl sólido. Determine a concentração mínima de íons cloreto (em molL-1 ) a partir da qual se iniciará o processo de precipitação de PbCl2.
Dado: Kps (PbCl2) = 1,6 x 10-5
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSubstâncias Inorgânicas: dissociação iônica e ionização, conceitos de ácido-base
Considere os dados da tabela abaixo:
![]()
De acordo com os dados acima, o ânion que atua como base mais forte é:
Provas
Uma solução de metilamina (CH3NH2) é preparada a 25ºC adicionando-se 0,05 mol dessa base orgânica em água suficiente para completar 500,0mL de solução. Sabendo que a 25ºC a constante de ionização básica (Kb) da metilamina é 3,6 x 10-4 , determine o pH aproximado da solução.
Dados: log 2 = 0,3 e log 3 = 0,48
Provas
Observe como variam as concentrações molares dos gases N2, O2 e N2O em uma reação realizada em sistema fechado.
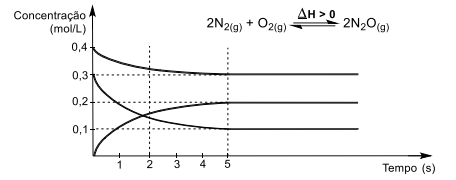
Sobre esse sistema reacional, é correto afirmar que:
Provas
Uma solução tampão é preparada a 25ºC a partir da mistura de 500,0mL de solução de ácido acético (CH3COOH) 1,0molL-1 com 500,0mL de solução de acetato de sódio (CH3COONa) 0,20molL-1 . Sabendo que, na mesma temperatura, a constante de ionização ácida (Ka) do ácido acético é 1,8 x 10-5 , determine o pH dessa solução.
Dado: log 3 = 0,48
Provas
Álcoois podem ter a hidroxila transformada em um bom grupo de saída após a formação do mesilato correspondente. Na sequência, é possível promover uma reação de eliminação em meio básico formando alquenos. A eliminação é favorecida quando a reação ocorre sob aquecimento e dois produtos são formados. Observe o esquema abaixo, em que as etapas descritas são representadas, utilizando-se o 2-heptanol como material de partida:
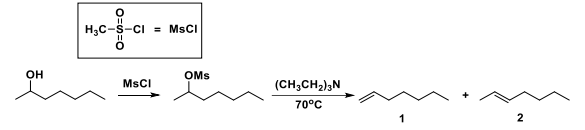
Sobre a etapa de eliminação, é correto afirmar que:
Provas
Caderno Container