Foram encontradas 40 questões.
O Estradiol, representado na figura a seguir, é um hormônio sexual feminino diretamente ligado à fertilidade da mulher. Como todo esteroide, é altamente solúvel em gorduras e apresenta uma estrutura básica de 17 átomos de carbono dispostos em quatro anéis ligados entre si, que formam diversos centros quirais.
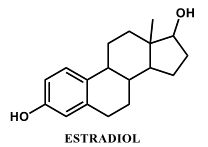
O número de centros quirais e o máximo de estereoisômeros presentes no estradiol são respectivamente:
Provas
- Química OrgânicaFunções Nitrogenadas: Amina, Amida, Nitrila, Isonitrila e Nitro Composto
- Química OrgânicaFunções Oxigenadas: Álcool, Fenol e Enol
- Química OrgânicaFunções Oxigenadas: Cetona, Aldeído, Éter, Éster, Ácido Carboxílico etc.
A seguir estão representados 3 alcalóides com suas respectivas ações farmacológicas. Esses alcaloides apresentam fórmulas estruturais semelhantes.
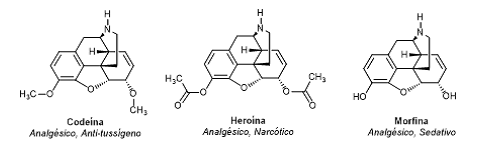
Os grupos funcionais presentes na codeína, heroína e morfina que diferenciam suas estruturas são respectivamente:
Provas
Uma das formas de produção da amônia é a partir da reação entre a cal viva (óxido de cálcio) e o cloreto de amônio, conforme reação a seguir:
CaO(s) + 2 NH4Cl(s) → 2 NH3(g) + H2O(g) + CaCl2(s)
10 g de uma amostra de cal viva foram colocados para reagir com excesso de cloreto de amônio e foram produzidos 5 g de amônia. Qual a porcentagem de óxido de cálcio dessa amostra de cal viva?
Dados: CaO (56 g mol-1 )
NH4Cl (53,5 g mol-1 )
NH3 (17 g mol-1 )
H2O (18 g mol-1 )
CaCl2 (111 g mol-1 )
Provas
- Química CinéticaRepresentação das Transformações Químicas
- Química CinéticaTransformações Químicas
- Química CinéticaVelocidade de Reação, Energia de Ativação e Catalisadores
O cloreto de titânio(IV), TiCl4, é um importante produto químico industrial. Esse pode ser usado tanto na obtenção do TiO2 quanto de titânio metálico. O TiCl4 pode ser obtido a partir de um minério contendo titânio (TiO2 impuro), utilizado em excesso, com carbono e gás cloro, conforme a equação química a seguir.
TiO2(s) + 2 Cl2(g) + C(s) → TiCl4(l) + CO2(g)
Considere que a obtenção do TiCl4 seja feita a partir de 852 g de C e 852 g de Cl2.
Dados: Cl2 (71 g mol-1 ); C (12 g mol-1 ) e TiCl4 (190 g mol-1 )
O reagente limitante e a massa em gramas de TiCl4 obtida são, respectivamente:
Provas
A utilização de um determinado elemento químico requer o conhecimento de suas propriedades. Para materiais condutores, por exemplo, são utilizados elementos metálicos, os quais podem ser moldados na forma de fios. As propriedades dos elementos, entre elas a condutividade, estão ligadas à sua configuração eletrônica de valência, que, por sua vez, pode ser obtida a partir dos valores sucessivos de energia de ionização (E.I). A partir da configuração eletrônica de valência, pode-se determinar a qual grupo da tabela periódica um elemento representativo pertence. Uma grande variação relativa do valor da E.I indica que o elétron é retirado de uma camada mais interna e os anteriores, consequentemente, da camada de valência. Observe os Quadros 1 e 2.
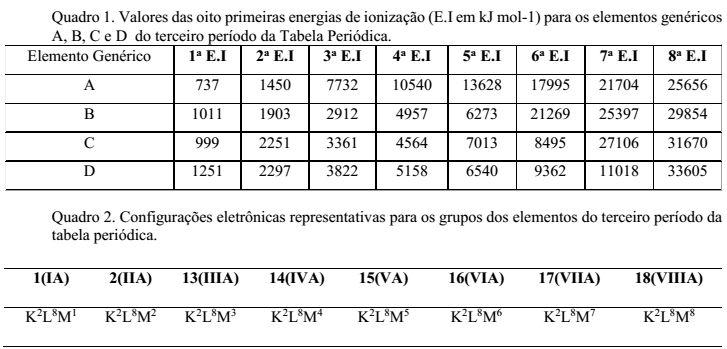
O elemento genérico adequado para obtenção de um fio condutor é:
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Uma _______________________ constitui uma excelente solução para a neutralização de soluções ácidas para descarte, pois além de elevar o pH, promove a formação de bolhas atóxicas que, quando cessadas, possibilitam que o usuário perceba que o meio já se encontra em pH próximo ao neutro.
A alternativa que completa a frase de forma CORRETA é:
Provas
Provas
- Sistemas de EquilíbrioSistemas Heterogêneos: Produto de Solubilidade (Kps)
- Sistemas de EquilíbrioSistemas Homogêneos: Solubilidade dos Sais, Hidrólise dos Sais e Curvas de Titulação.
Íons Ba2+(aq) são altamente tóxicos e suas soluções não podem ser descartadas na rede de esgoto. Esses íons devem, portanto, ser removidos de misturas que se pretende descartar, o que pode ser feito através de reações de precipitação. Para a remoção de íons Ba2+(aq) de 1,0 L de resíduo de concentração 0,01 mol L -1 foram propostos os seguintes procedimentos:
I. Adição de 0,1 L de solução de Na2CO3 0,1 mol L-1
II. Adição de 0,1 L de solução de Na2SO4 0,1 mol L-1
III. Adição de 0,1 L de solução de Na3PO4 0,01 mol L-1
IV. Adição de 0,1 L de solução de NaOH, 0,01 mol L-1
Dado: Constante do produto de solubilidade dos compostos de bário (Ks)
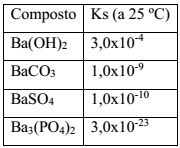
O procedimento que resulta na produção de um material mais adequado ao descarte é:
Provas
- Química CinéticaRepresentação das Transformações Químicas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
O ácido oxálico (H2C2O4 . 2H2O) é um ácido diprótico muito usado para fins analíticos, industriais e aplicações veterinárias. Uma amostra de 0,2520 g de um ácido oxálico foi pesada e titulada completamente com 25,00 mL de uma solução de NaOH de concentração 0,1200 mol L-1 .
Dado: H2C2O4 . 2H2O = 126 g mol-1
A porcentagem de pureza desse ácido é:
Provas
- FundamentosPropriedades das Substâncias
- Química InorgânicaGeometria Molecular, Polaridade e Forças Intermoleculares
A estrutura de uma molécula ou íon é descrita em função dos seus ângulos de ligação e comprimentos de ligação. Considere o dióxido de nitrogênio e seus respectivos íons NO2+ e NO2- .
Dado: N (Z = 7); O (Z = 8)
A ordem CRESCENTE dos ângulos de ligação O-N-O nessas espécies é:
Provas
Caderno Container