Foram encontradas 180 questões.
Em uma blitz policial, o carro de um motorista foi revistado, encontrando-se um sólido branco suspeito que apresentou resultado positivo para alcaloide. Se a substância encontrada for a codeína, o motorista será liberado, se for a morfina, o motorista precisa apresentar receita médica que justifique o porte de tal substância, e se for a heroína, o motorista será preso.
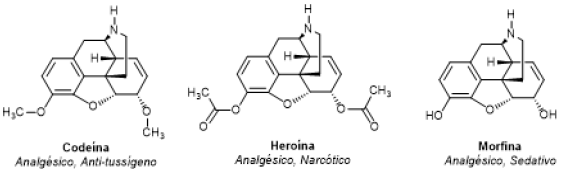
Seria possível inferir se o motorista cometeu alguma infração ou irregularidade utilizando uma análise de infravermelho?
Provas
Cavernas próximas a regiões com solo rico em calcário podem formar estalactites com o passar dos anos. Sua formação pode ser representada pela equação:
CaCO3 (s) + CO2(g) + H2O (l) ⇌ Ca2+ (aq) + 2 HCO3 - (aq)
Dentre as seguintes condições:
I. Evaporação constante da água;
II. Corrente de ar frio e úmido;
III. Elevação da temperatura no interior da caverna;
IV. Visitas frequentes de grandes grupos de pessoas.
Quais favorecem a formação de estalactites?
Provas
Provas
- Química CinéticaRepresentação das Transformações Químicas
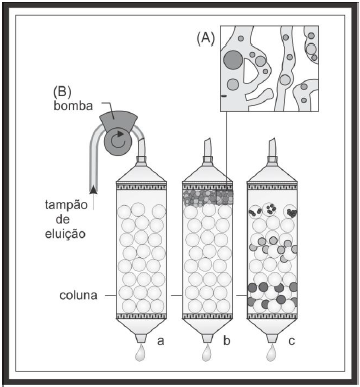
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Um frasco de ácido clorídrico concentrado contém 37% de HCl em massa e apresenta uma densidade de 1,20 g mL-1 . Foi transferido 5,00 mL de HCl desse frasco para um balão volumétrico de um litro e avolumado com água deionizada.
Qual o volume necessário dessa solução de HCl diluída para neutralizar 500 mL de NaOH 0,02 mol L-1 ?
Provas
- FundamentosLigações Químicas
- FundamentosPropriedades das Substâncias
- Química CinéticaTransformações Químicas
Gráficos de energia potencial para a formação de moléculas ou íons moleculares são bastante úteis, pois podem ser utilizados para a obtenção de parâmetros importantes como distância de ligação (DL) e energia de ligação. Observe o gráfico a seguir.
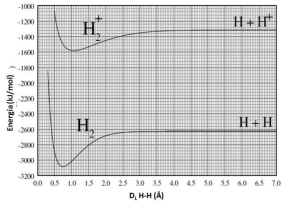
A partir das informações que podem ser extraídas do gráfico, é CORRETO afirmar que:
Provas
- FundamentosLigações Químicas
- FundamentosPropriedades das Substâncias
- Química CinéticaRepresentação das Transformações Químicas
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
- Sistemas de EquilíbrioSistemas Homogêneos: Equilíbrio Iônico: Conceitos, Diluição de Ostwald, Efeito do Íon Comum
Um copo, com capacidade de 250 mL, contém 100 mL de uma solução aquosa 0,10 mol L-1 de ácido acético na temperatura de 25°C. Após a adição de mais 100 mL de água pura a essa solução, com a temperatura permanecendo constante, as consequências sobre a concentração de íons acetato (mol L-1) e quantidade de íons acetato (mol), respectivamente são:
Dados: Ka = 1,8.10-5, √1,8x10-6 = 0,0013 e √9x10-7 = 0,0095.
Provas
- FundamentosLigações Químicas
- FundamentosPropriedades das Substâncias
- Química CinéticaTransformações Químicas
A Teoria do Orbital Molecular (TOM) permite prever a existência de espécies, como íons moleculares,sua estabilidade relativa e algumas propriedades. Entretanto a TOM não prevê a existência da espécie He2. Porém essa espécie existe apenas à temperatura de 4,5 K, possuindo comprimento de ligação de 52 angstrons e energia de ligação de 9,63x10-3J mol-1 determinados experimentalmente. Com base na TOM,avalie as afirmações a seguir.
Dado He (Z = 2)
I. A espécie He2 possui ordem de ligação igual a zero e é estável.
II. Ordem de ligação no íon molecular He2+é menor que no dímero de hélio
III. O comprimento de ligação do He2+é menor que do He2.
IV. As energias dos orbitais moleculares 1σg e 1σu do He2+e H2+ são as mesmas.
Assinale a alternativa que apresenta somente as afirmações CORRETAS:
Provas
A constante de equilíbrio KC para a seguinte reação é 0,80 a uma dada temperatura. Um recipiente de 5,00L contém 0,4 mol de FeBr3, 0,5 mol de FeBr2 e 0,4 mol de Br2 nessa temperatura.
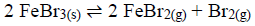
Com base no exposto, assinale a alternativa CORRETA.
Provas
Provas
Caderno Container