A reação de Landolt, conhecida como Relógio de Iodo, é
um clássico experimento de cinética química que permite
compreender como a alteração de fatores experimentais
influencia na velocidade das reações químicas.
Nesse sistema, o peróxido de hidrogênio (H₂O₂), em meio
ácido, oxida íons iodeto (I⁻) obtidos de uma solução de
iodeto de potássio (KI), produzindo iodo molecular (I₂),
conforme a reação a seguir representada.
H2O2 (aq) + 2I⁻ (aq) + 2H⁺(aq) → I2 (aq) + 2H2O (l)
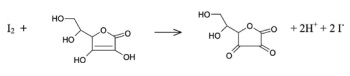
O iodo formado pode reagir com a vitamina C (ácido
ascórbico, C₆H₈O₆), que atua como agente redutor,
convertendo-o novamente em íons iodeto e originando
ácido dehidroascórbico (C₆H₆O₆), conforme a
reação subsequente.
A partir dessas informações e considerando-se que M KI = 166 g·mol-1 seja a massa molar do iodeto de potássio, M H2O2 = 34 g·mol-1 seja a massa molar de peróxido de hidrogênio e que a constante de Avogadro valha 6 × 1023 mol−1, julgue o item a seguir.
Assumindo-se que 1 mol de vitamina C é consumido para cada mol de H₂O₂, em uma solução contendo 0,0010 mol·L⁻¹ de C₆H₈O₆, se o tempo de reação for 20 segundos, então a velocidade média da reação, em relação à vitamina C, será inferior a 4,0 × 10⁻⁵ mol·L⁻¹·s⁻¹