Para ocorrer uma reação química entre duas substâncias, é preciso fornecer certa quantidade de energia, geralmente na forma de calor, que favoreça o encontro e a colisão entre tais substâncias. A energia também é necessária para romper ligações químicas existentes entre os átomos de cada substância, favorecendo, assim, a ocorrência de outras ligações químicas e a síntese de uma nova substância a partir de duas iniciais.
O “caminho” da energia do processo é mostrado no diagrama abaixo.
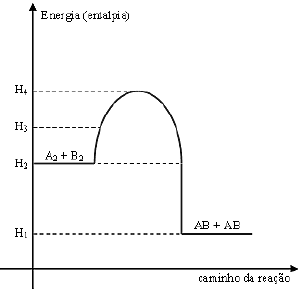
A coluna da esquerda apresenta dados energéticos característicos do andamento da reação (quantidades de energia das respectivas etapas da reação) (H1 a H4) e a da direita, a especificação de cada um deles.
Numere a coluna da direita de acordo com a da esquerda.
1 - H1
2 - H2
3 - H3
4 - H4
( ) A energia do sistema é maior, mas ainda insuficiente para que ocorra uma colisão efetiva.
( ) A energia, nesse ponto, é suficiente para a reação. Dá-se aqui a formação de um estado de transição.
( ) As moléculas do produto (AB) estão definitivamente formadas.
( ) As moléculas reagentes (A2 e B2) não possuem energia suficiente para reagirem.
Marque a sequência correta.