H2(g) + ½ O2(g) → H2O(g)
| T (K) |
!$ \Delta !$H (KJ) | !$ \Delta !$S (J/K) | !$ \Delta !$G (KJ) |
| 300 | -242 | -44 | -229 |
| 350 | -242 | -46 | -226 |
| 400 | -243 | -47 | -224 |
| 450 | -243 | -48 | -222 |
| 500 | -244 | -50 | -220 |
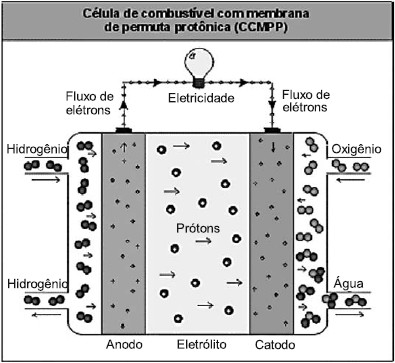
O esquema e a tabela acima mostram, respectivamente, uma célula de combustível e os dados termodinâmicos para a reação. À pressão atmosférica e a 500K, a célula opera gerando uma d.d.p. entre os eletrodos de 1,0V. Qual a estimativa da quantidade de calor gerada pela célula, em KJ/mol de H2O?
| R = 8 J.mol-1K-1 !$ \quad \quad !$ F=100.000 C |
Provas
Questão presente nas seguintes provas