Ao oxidarmos uma placa de zinco em
ácido nítrico ocorre um processo de oxidação.
Em relação a esse processo e o potencial de
redução a 25 °C e sendo dados,
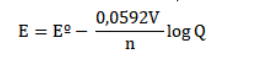
Zn +2 (aq) /Zn (s) = - 0,763 V NO 3 - /NO (g) = 0,96 V P NO (g) = 2,0 atm [H + ] = 1,0 mol/L [Zn +2 ] = 1,0 mol/L [NO 3 - ]= 1,0 mol/L
têm-se:
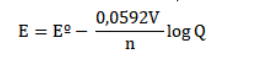
Zn +2 (aq) /Zn (s) = - 0,763 V NO 3 - /NO (g) = 0,96 V P NO (g) = 2,0 atm [H + ] = 1,0 mol/L [Zn +2 ] = 1,0 mol/L [NO 3 - ]= 1,0 mol/L
têm-se: