A equação (1) estabelece a lei dos gases ideais, que pode ser reescrita no formato demonstrado pela equação (2), através do volume especifico v = V/m e da constante de um gás particular !$ R=\overline{R}/M !$, Nessas equações V representa o volume, m a massa do sistema, !$ \overline{R} !$ a constante universal dos gases, p a pressão, Ta temperatura e M a massa molar do gás.
!$ pV=n \overline{R}T={\large{m \over M}}\overline{R}T !$ (1)
!$ p\left({\large{V \over m}}\right)=\left({\large{\overline{R} \over M}} \right)T !$ (2)
Para gases ideais, o trabalho específico !$ W_{i,f}=W_{i,f}/m !$ realizado pelo sistema em um processo isotérmico que vai do estado inicial (i) para o final (f) é dado por:
!$ W_{i,f}=p_iv_i ln \left({\large{v_f \over v_i}} \right) !$ (3)
Considere como sistema o CO2 (R = 0,1889kJ /(kgK) ), admitido como gás ideal contido em um dado cilindro, realizando o ciclo mostrado no diagrama p - V . Calcule a massa do gás, considerando que o trabalho realizado pelo sistema do processo que vai do estado 3 para o estado 1 é dado por W3,1 = 674,3730k|J / K, que a razão dos volumes nos estados 2 e 1 é !$ {\large{V_2 \over V_1}}=0,5 !$, que a temperatura no estado 3 é de T3=327ºC.
Dados: ln(2) = 0,7; e 0ºC equivalente a - 273K
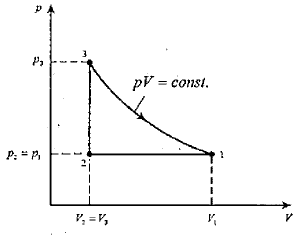
Figura - Diagrama p - V