Uma alternativa sustentável para suprir a demanda energética atual é o uso de células a combustível, que são capazes de produzir eletricidade diretamente a partir de uma reação química, como numa bateria, mas usam reagentes que são fornecidos continuamente, como num motor. No entanto, as células a combustível fazem uso mais eficiente dos recursos, porque pouca energia é desperdiçada na forma de calor. A figura a seguir ilustra, esquematicamente, uma célula a hidrogênio.
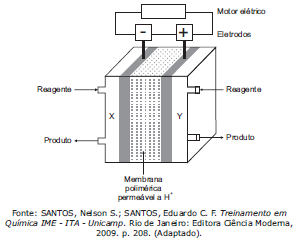
Esta célula é alimentada por hidrogênio e oxigênio gasosos e opera segundo as seguintes semirreações:
| H2(g) 2H+ (aq) + 2e- E° = 0,00 V |
| O2(g) + 4H+(aq) + 4e- → 2H2O(I) E° = +1,23 V |
Analise as seguintes afirmativas:
I → Este processo não é termodinamicamente espontâneo.
II → O oxigênio é oxidado pelo meio ácido neste processo.
III → O compartimento X é abastecido por hidrogênio.
IV → A proporção H:O, em massa, para o processo global é 1:8.
Está(ão) correta(s)