Considere quando necessário:
Densidade da água = 1 g/ml
Temperatura de ebulição da água = 100°C
Temperatura de fusão da água = 0°C
R = 0,082 atm.L. mol-1K-1 = 8,3J.K-1.mol-1.
Número de Avogrado = 6, 022 x 1023
1 Faraday = 96500 C
Pressão de vapor da água pura a 28°C = 28,0 torr
Ln 2 = 0,39
A pressão osmótica pode ser definida como a pressão externa que deve ser aplicada a uma solução concentrada para evitar a osmose. Considere as figuras abaixo representadas. Elas traduzem quatro soluções aquosas de composição e concentração variadas, depositadas em um recipiente transparente. Considere, ainda, que as espécies iônicas estão 100% ionizadas:
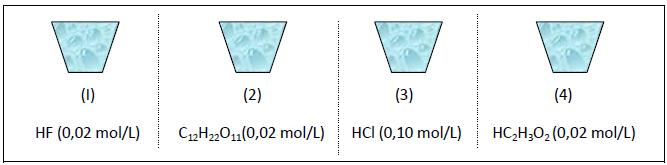
Assinale a alternativa que melhor indica a pressão osmótica (!$ \pi !$) das quatro soluções.