Para responder a questão, utilize o enunciado a seguir.
Diversas aplicações industriais de soluções exploram, simplesmente, os efeitos da presença de partículas de umsoluto num sistema, independentemente da sua natureza. Uma das situações mais familiares é a adição de etilenoglicol (“anticongelante”) ao líquido de arrefecimento dos radiadores dos carros. Isto é necessário, pois o congelamento da água no motor pode provocar danos na estrutura devido à expansão da água (aumento de volume) durante o congelamento. O etilenoglicol diminui a temperatura de congelamento da água (crioscopia), prevenindo o congelamento em dias de temperatura abaixo de 0 °C; este aditivo também aumenta o ponto de ebulição (ebulioscopia) permitindo que o sistema do motor opere acima de 100 ºC sem criar altas pressões; a pressão de vapor também diminui (tonoscopia), e o fluxo de solvente é afetado quando uma solução é separada do solvente puro por uma membrana semipermeável (osmose). Estas são propriedades coligativas de soluções.
A figura a seguir mostra a variação da pressão de vapor em função da fração molar de benzeno (XC6H6) a 20 °C para um sistema benzeno/tolueno.
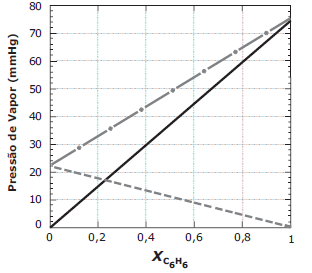
Fonte: AVERILL, Bruce, A., ELDREDGE, Patricia. General Chemistry.
Irvington: Flat World Knowledge Inc., 2003, pag. 895. (Adaptado)
De acordo com os dados fornecidos, analise as afirmações a seguir.
I → A pressão de vapor total (Pt), representada por uma das linhas, é igual a soma da pressão parcial de vapor dos componentes, caracterizando uma solução ideal que obedece a Lei de Raoult.
II→As forças intermoleculares nos dois líquidos são de natureza e magnitude completamente distintas, contribuindo para a formação de uma solução ideal.
III → A pressão de vapor do tolueno a 20 ºC é 22,3 mmHg, enquanto a do benzeno é 74,7 mmHg sob as mesmas condições. Isto implica que o benzeno é mais volátil do que o tolueno.
IV → Na presença de tolueno, o benzeno tem maior tendência a evaporação quando comparado a ele puro.
Está(ão) correta(s)