O modelo atômico de Bohr, que foi elaborado para contornar as dificuldades encontradas pelos modelos clássicos de Thomson e Rutherford, foi fundamentado em alguns postulados e apresentava concordância com os dados espectrais do átomo de Hidrogênio.
Para esse modelo, a energia de cada órbita do átomo de hidrogênio é dada por !$ E_n = { \large 13,6 \over n^2} e V !$.
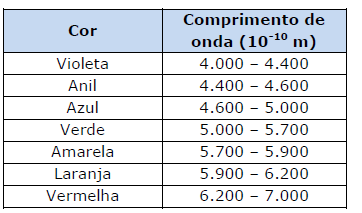
De acordo com a equação acima, com a tabela ao lado e considerando-se que !$ 1eV = 1,6X10^{-19} J, h = 6,63X10^{-34} J.s !$ e !$ c = 3X10^8 m/s !$, afirma-se que a cor de um fóton emitido num salto quântico do segundo estado excitado para o primeiro estado excitado do átomo de hidrogênio é