O hidróxido de alumínio !$ (A\ell (OH)_3) !$, ao precipitar em solução aquosa, forma um sólido gelatinoso que pode ser usado como agente floculante no tratamento de água. Essa precipitação pode ocorrer pela adição de um hidróxido solúvel a uma solução aquosa ácida contendo um sal de alumínio solúvel, como o !$ A\ell C\ell_3 !$. Entretanto, adicionando-se excesso de hidróxido ao meio, há a formação de íons !$ A\ell (OH)_4^- !$, espécie solúvel em água, e o precipitado se solubiliza novamente. Dessa forma, dependendo do pH do meio, uma dentre as espécies !$ A\ell (OH)_4^- (aq) !$, !$ A\ell^{3+} (aq) !$ e !$ A\ell^{3+} (aq) !$ estará presente na solução em quantidade maior que as demais, como exemplificado no esquema.
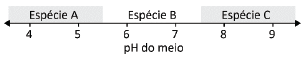
A alternativa que mostra corretamente qual das espécies estará em quantidade maior que as duas outras em cada faixa de pH é: