Considere o texto abaixo e a Tabela para responder à questão.
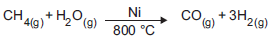
Com o objetivo de se diminuírem os prejuízos ambientais, novas fontes de energia vêm ganhando cada vez mais espaço. As células ou pilhas a combustível são dispositivos silenciosos que transformam energia química em energia elétrica, como em uma bateria, utilizando um combustível que é fornecido de forma contínua, como em um motor. No futuro, essa fonte de energia limpa deverá ser muito empregada em veículos e estações geradoras de energia em residências, hospitais e pequenas indústrias. Atualmente, o combustível mais atraente é o hidrogênio, pois gera apenas água como produto final. As principais fontes geradoras de hidrogênio são: gás natural (metano), metanol, etanol e água. O gás natural é o maior produtor de hidrogênio. Neste, o metano é transformado em hidrogênio e monóxido de carbono, de acordo com a reação a seguir.
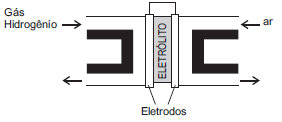
A estrutura básica das células a combustível consiste em dois eletrodos porosos (platina ou níquel), separados por um eletrólito e conectados por meio de um circuito externo, conforme mostrado no esquema abaixo:
Potenciais padrão do eletrodo
| Semirreação de redução |
Potencial padrão do eletrodo a 25 °C |
| !$ O_{2(g)} + 4H^+_{(aq)} + 4e^- \rightarrow 2H_2O_{(l)} !$ | + 1,23 V |
| !$ O_{2(g)} + 2H_2O_{(l)} + 4 e^- \rightarrow 4OH^- _{(aq)} !$ | + 0,40 V |
| !$ 2H^+_{(aq)} + 2e^- \rightarrow H_{2(g)} !$ | 0,00 V |
| !$ 2H_2O_{(l)} + 2 e ^- \rightarrow H_{2(g)} + 2OH^-_{(aq)} !$ | 0,83 V |
Existem diversos tipos de eletrólitos usados nas células a combustível. Soluções aquosas de hidróxido de potássio, ácido ortofosfórico concentrado, óxidos sólidos como o óxido de zircônio IV, carbonatos fundidos (mistura de carbonatos de lítio e sódio) e até membranas poliméricas. As fórmulas químicas que representam, respectivamente, o ácido e o óxido mencionados no texto são