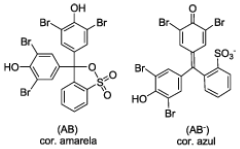
Diversos compostos exibem colorações que dependem do pH da solução na qual estão dissolvidos. Muitos desses compostos são utilizados para indicar a acidez ou alcalinidade de soluções aquosas e são chamados de indicadores ácido/base. Um indicador ácido/base é uma base ou ácido orgânico fraco cuja coloração é diferente da coloração de seu ácido ou base conjugados. Abaixo são mostradas duas formas (dissociada e não-dissociada) do indicador azul de bromotimol (pKa = 7,10) e suas respectivas colorações. Com base no texto acima e nas estruturas abaixo, marque (V) para as alternativas verdadeiras e (F) para as falsas.
( ) Com base no valor do pKa do azul de bromotimol, é possível afirmar que sua faixa de transição de pH é de 1,2 a 2,8.
( ) O azul de bromotimol é classificado como um indicador do tipo ácido (HIn) e o seu comportamento em meio aquoso é dado pela equação HIn + H2O In- + H3O+.
( ) Diversos fatores influenciam a faixa de transição de um indicador, como a temperatura e a força iônica do meio.
( ) O azul de bromotimol adquire coloração amarela em pH = 10.
( ) Ambas as formas do azul de bromotimol apresentadas possuem a função orgânica álcool em suas estruturas.
Site da revista Química Nova
Assinale a alternativa que contém a sequência CORRETA, de cima para baixo.