Em uma aula prática de química, foi montada a aparelhagem representada na figura a seguir, para um experimento de eletrólise, usando-se como eletrólito, uma solução aquosa de iodeto de sódio 1,0 mol/L em pH = 7 e algumas gotas de uma solução aquosa de amido.
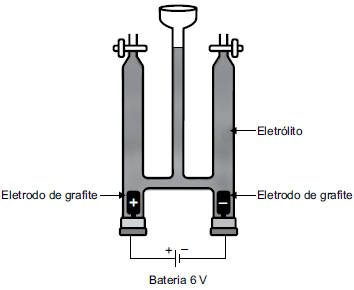
Dados: potencial padrão de redução a 25 ºC.
!$ O_2(g) + H_2O ( \ell) + 4e^- \rightarrow 4 OH^-(aq)\,\,\,\,E^{ \circ} + 0,40\,V\\I_2(s) + 2e^- \rightarrow I^- (aq)\,\,\,\,\,E^{ \circ} = + 0,54\,V\\O_2(g) + 4 H^+(aq) + 4e^- \rightarrow 2\,H2O(I)\,\,\,\,E^{ \circ} = + 1,23\,V\\2\,\,H_2O ( \ell) + 2e^- \rightarrow H_2(g) + 2OH^-(aq)\,\,\,\,\,E^{ \circ} = -0,83\,V\\Na^+(aq) + 1e^- \rightarrow Na(s)\,\,\,\,\,\,E^{ \circ} = -2,71\,V !$
(P. Atkins, P.; L. Jones; Princípios de
Química: questionando a vida moderna e o meio ambiente. 5ª ed. Porto Alegre: Bookman, 2012)
Ao iniciar o experimento, verificou-se o sugimento de coloração azulada em um dos compartimentos eletródicos e a formação de um gás no outro compartimento. Esse fato ocorreu devido à formação de iodo no