- Química InorgânicaSoluções e Substâncias InorgânicasSubstâncias Inorgânicas: dissociação iônica e ionização, conceitos de ácido-base
A compreensão dos conceitos de ácidos e bases é fundamental para a química e tem sido moldada por diferentes teorias ao longo do tempo. A teoria de Arrhenius, proposta no final do século XIX, define ácidos como substâncias que liberam íons de hidrogênio (H+) em solução aquosa e bases como substâncias que liberam íons hidroxila (OH-) em solução aquosa. Em contrapartida a teoria de Bronsted-Lowry, desenvolvida em 1923, ampliou essa definição ao considerar ácidos como doadores de prótons e bases como receptores de prótons, independente da presença de água. Ambas as teorias são fundamentais para o entendimento das propriedades ácido-base e são aplicadas em diversos campos da química.
A seguir, observe as reações:
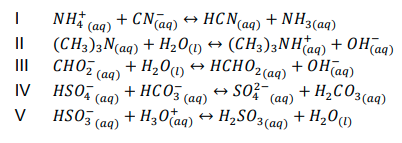
Em relação a Teoria de Bronsted-Lowry e as reações dadas anteriormente, julgue as afirmativas abaixo como V para verdadeiro e F para falso.
( ) Nas reações I, III e IV o NH+ 4, H2O e HSO-4, respectivamente, são ácidos.
( ) Ambas as reações II e III possuem o mesmo ácido, mas com base conjugada diferente.
( ) A reação V apresenta H3O+ como ácido e HSO-3 como base.
( ) A reação I tem como ácido CN- , ácido conjugado o HCN e a base conjugada NH3.
( ) Dentre as cinco reações, há uma entre elas com o OH- como sendo seu ácido conjugado.
Qual das seguintes alternativas apresenta a sequência CORRETA?