Durante o curso de formação, um dos experimentos de investigação realizados pelos alunos da EsPCEx, utilizando o conceito de proteção por meio de ânodo de sacrifício, consiste em polir quatro pregos de ferro, envolver cada um deles com uma fita metálica de diferentes metais e mergulhá-los em uma solução aquosa de ferricianeto de potássio com oxigênio dissolvido. O ferricianeto de potássio é um sal que, em meio aquoso, atua como um indicador de corrosão do ferro, pois adquire coloração azul na presença de íons de ferro. O experimento está representado na imagem abaixo:
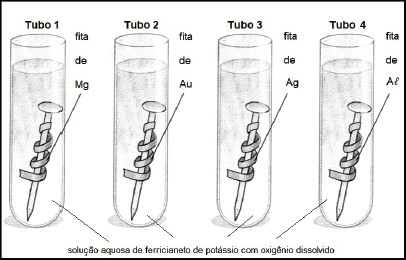
Adaptado de: USBERCO, João; SALVADOR, Edgard. Química. 12. ed. São Paulo: Editora Saraiva, 2009, v. 2, p. 296.
Dados:
| Potenciais padrão de redução |
E0 (T = 298,18 K) |
Potenciais padrão de redução |
E0 (T = 298,18 K) |
| Mg2+ (aq) + 2 e- → Mg (s) |
E0 = – 2,37 V |
A\( \ell \)3+(aq) + 3 e- → A\( \ell \) (s) | E0 = – 1,67 V |
| Au3+ (aq) + 3 e- → Au (s) |
E0 = + 1,50 V |
Fe2+ (aq) + 2 e- → Fe (s) |
E0 = – 0,44 V |
| Ag+ (aq) + 1 e- → Ag (s) |
E0 = + 0,80 V |
2H2O (l) + O2 (g) + 4 e- → 4 OH- (ag) |
E0 = + 0,40 V |
Considerando as informações apresentadas, após certo tempo, surgirá coloração azul apenas nos tubos