- Química CinéticaRepresentação das Transformações Químicas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
O gás dióxido de enxofre é um dos principais poluentes atmosféricos que afetam a vida do homem. Para quantificá-lo na atmosfera, o analista químico, inicialmente, monta um sistema para coletar o dióxido de enxofre, utilizando um borbulhador, isto é, um frasco contendo solução de peróxido de hidrogênio, onde o ar atmosférico é borbulhado com o auxílio de uma bomba que o aspira. A figura a seguir representa um tipo de borbulhador e dispositivos usados na coleta da amostra de ar a ser analisada. No cálculo da concentração do gás em estudo, é importante medir o volume de ar da amostra por meio de um totalizador de volume que mede todo o ar que passou pelo borbulhador. Finalizada a amostragem, o analista químico determina a quantidade de ácido sulfúrico formado no borbulhador, titulando-o com solução de base forte NaOH, por exemplo, e calcula a quantidade proporcional de dióxido de enxofre. Utilizando-se o volume total do ar amostrado, é possível, então, calcular a concentração de dióxido de enxofre na amostra de ar.
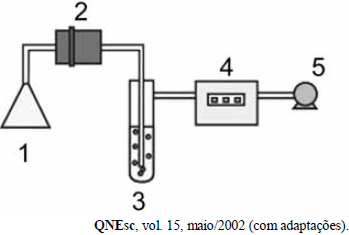
Sistema para dosagem do SO2: 1– entrada de ar em forma de funil; 2 – filtro para retenção das partículas; 3 – borbulhador contendo solução de água oxigenada; 4 – totalizador de volume para medida do ar total amostrado; 5 – bomba para aspirar o ar.
Considere que a seguinte reação ocorra no borbulhador.
SO2(g) + H2O2(l) → H2SO4(aq)
Com base nas informações acima, julgue os itens de 101 a 104.
Considerando que, na titulação do ácido sulfúrico formado no borbulhador, foram gastos 3,2 mol de NaOH e que o totalizador de volume indicou 4 m3 de amostra de ar, conclui-se que, nessa análise, a concentração de dióxido de enxofre no ar amostrado era de 8 × 10-4 mol / L.