Texto para a questão
Se uma amostra for fortemente iluminada por uma determinada luz que o material seja capaz de absorver, este poderá reemitir luz fluorescente. A fluorescência decorre do decaimento radiativo dos átomos entre dois níveis de energia bem definidos E2 e E1 por exemplo.
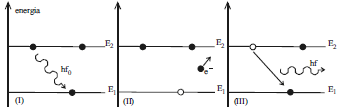
O diagrama acima mostra que um determinado fóton de luz absorvido por um elétron (figura I) pode ser ejetado (fotoelétron), deixando uma vacância no nível energético E1 (figura II) que pode ser ocupado por um elétron do nível E2 emitindo um fóton fluorescente de energia hf (figura III). Considere que h = 6,63 × 10-34 JAs = 4,14×10-15eVAs é a constante de Planck e f é a frequência do fóton dada por: !$ f = { \large E_2 - E_1 \over h} !$
Considerando que, para o átomo de hidrogênio, os níveis de energia são !$ E_n = { \large 13,58 \over n^2} !$ e V, o fóton fluorescente infravermelho da transição da camada P para a camada N tem comprimento de onda 8, em :m, entre