Considere quando necessário:
Densidade da água = 1 g/ml
Temperatura de ebulição da água = 100°C
Temperatura de fusão da água = 0°C
R = 0,082 atm.L. mol-1K-1 = 8,3J.K-1.mol-1.
Número de Avogrado = 6, 022 x 1023
1 Faraday = 96500 C
Pressão de vapor da água pura a 28°C = 28,0 torr
Ln 2 = 0,39
Quando um soluto sólido começa a se dissolver em um solvente, a concentração de partículas do soluto na solução aumenta, bem como suas chances de colidir com a superfície do sólido. Tal colisão pode fazer com que a partícula do soluto se religue ao sólido. Esse processo é chamado de cristalização. Um técnico em química preparou 320g a 60°C de solução saturada de um sal, cuja solubilidade em água está expressa na tabela abaixo. Em seguida, resfriou o sistema para 20°C e notou que houve cristalização do sal sólido.
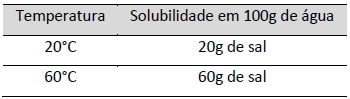
Tendo filtrado o sistema e pesado o precipitado, qual a massa de sal sólido obtida pelo técnico?