A bateria de Thomas Edison desenvolvida no século 19 é um dispositivo eletroquímico que funciona de acordo com o esquema simplificado representado na figura. No sentido da descarga, o potencial fornecido por par de eletrodos é igual a +1,35V.
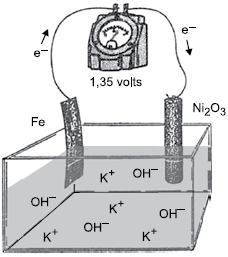
(George C.Pimentel. “Química Ciência Experimental” 1981. Adaptado)
Considere as informações:
|
Semirreação |
Potencial padrão de redução (Eº) |
|
I.!$ Fe (OH)_2 (s) + 2e^- \rightarrow Fe(s) + 2OH^-(aq) !$ |
X |
| II.!$ Ni_2O_3(s) + 3 H_2 O ( \ell) + 2e^- \rightarrow 2 Ni(OH)_2 (s) = 2OH^-(aq) !$ |
+0,48V |
Na bateria de Thomas Edison em operação no sentido da descarga, o eletrodo em que se processam a oxidação e o potencial padrão de redução da equação I são:
Provas
Questão presente nas seguintes provas