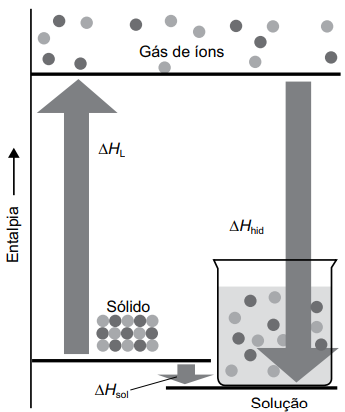
A figura representa um diagrama das entalpias envolvidas na formação de uma solução aquosa a partir de um soluto sólido iônico cristalino.
A entalpia de solução (∆Hsol) é o resultado da soma da entalpia de rede cristalina (∆HL) e a entalpia de hidratação (∆Hhid)
(ATKINS, Peter; LORETTA, Jones, LAVERMAN, Leroy. Princípios de Química: questionando a vida moderna e o meio Ambiente. 2. ed. Porto Alegre: Bookman, 2006)
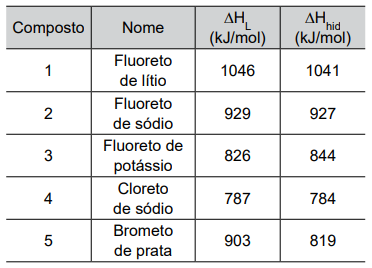
A tabela apresenta os valores, em módulo, de entalpia de rede (∆HL) e entalpia de hidratação (ΔHhid) de alguns sais.
(ATKINS, Peter; LORETTA, Jones, LAVERMAN, Leroy. Princípios de Química: questionando a vida moderna e o meio Ambiente. 2. ed. Porto Alegre: Bookman, 2006)
O diagrama de energia da figura é compatível ao processo de dissolução do composto
A entalpia de solução (∆Hsol) é o resultado da soma da entalpia de rede cristalina (∆HL) e a entalpia de hidratação (∆Hhid)

(ATKINS, Peter; LORETTA, Jones, LAVERMAN, Leroy. Princípios de Química: questionando a vida moderna e o meio Ambiente. 2. ed. Porto Alegre: Bookman, 2006)
A tabela apresenta os valores, em módulo, de entalpia de rede (∆HL) e entalpia de hidratação (ΔHhid) de alguns sais.

(ATKINS, Peter; LORETTA, Jones, LAVERMAN, Leroy. Princípios de Química: questionando a vida moderna e o meio Ambiente. 2. ed. Porto Alegre: Bookman, 2006)
O diagrama de energia da figura é compatível ao processo de dissolução do composto