- Sistemas de EquilíbrioSistemas Homogêneos: Solubilidade dos Sais, Hidrólise dos Sais e Curvas de Titulação.
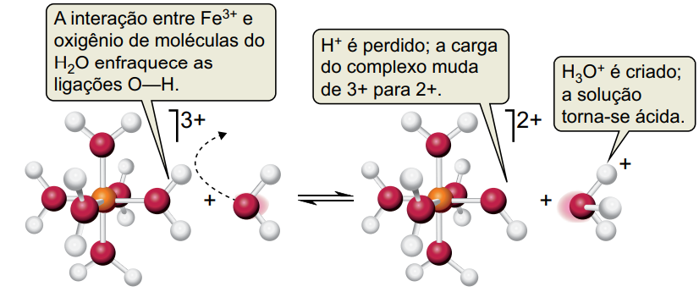
Considere a figura que mostra o mecanismo da reação de íons metálicos hidratados com a água, o exemplo é para o íon [Fe(H2O)6]3+, e a tabela de constantes de acidez (Ka) para cátions metálicos em solução aquosa, a 25 °C a seguir:
Figura
Tabela
| cátion | Ka |
|---|---|
| Zn2+ | 2,5x10–10 |
| Ni2+ | 2,5x10–11 |
| Cr2+ | 1,6x10–4 |
(Brown, T. L.; LeMay Jr, H. E.; Bursten, B. E.; Burdge, J. R. Química, a ciência central, 2005)
De acordo com a tabela e o mecanismo apresentado na figura, conclui-se que os íons metálicos hidratados se comportam como __________ e a solução que apresenta maior pH é a que contém os íons hidratados __________.
As lacunas são preenchidas, correta e respectivamente, por: