Através do cálculo da variação de entalpia de formação (ΔHf) de um composto iônico, é possível prever a existência de um determinado composto. A tabela abaixo mostra os valores da entalpia de cada etapa para a possível formação de um composto genérico AB e BA.

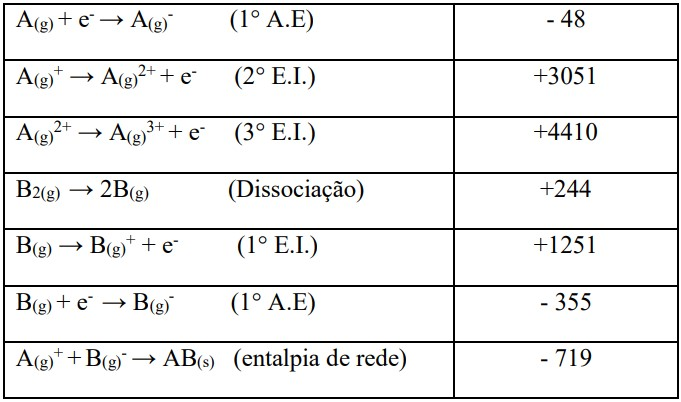
Considere as informações do quadro acima e avalie as afirmativas abaixo:
I - O elemento A, provavelmente, pertence ao grupo 2 da tabela periódica.
II - O valor da entalpia de formação do sólido AB é igual a -438 kJ/mol.
III - O fator que governa a formação espontânea do produto AB é entálpico, já que a entropia para a formação de ligação química é desfavorecida.
IV - A entalpia de formação do produto BA seria igual a +695 kJ/mol, considerando o mesmo valor de entalpia de rede da formação de AB. O fator determinante que torna a formação do composto BA não espontânea é a baixa afinidade eletrônica de A.
Assinale a alternativa com as afirmações CORRETAS.