Complexos são termodinamicamente mais estáveis quando formados por agentes quelantes, que são ligantes polidentados, em comparação a um número equivalente de ligantes monodentados. Um exemplo importante na medicina é a aplicação de agentes quelantes para a remoção seletiva de íons metálicos tóxicos como Hg2+ e Pb2+, preservando os metais biologicamente importantes.
As figuras abaixo mostram alguns exemplos de ligantes quelantes:
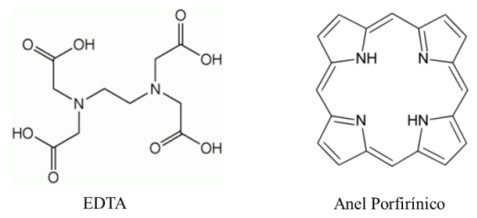
Com base na estabilidade dos íons complexos e agentes quelantes, analise as afirmações abaixo:
I. A constante de formação do quelato é extremamente alta quando comparada a ligantes monodentado de mesma natureza. Isso se deve à energia livre de Gibbs ser mais negativa, sendo governada pelo efeito entálpico em detrimento ao efeito entrópico.
II. O EDTA é um ácido poliprótico cuja estrutura pode ser dada pela fórmula H4Y, um quelante hexadentado muito utilizado na indústria de alimentos e na medicina. O EDTA forma complexos octaédricos com o centro metálico.
III. Quelatos com íons metálicos das séries mais elevadas tendem a ser mais lábeis, o que pode explicar a preferência de ligantes quelantes por íons como Hg2++ e Pb2+ .
IV. Os anéis porfirínicos possuem 4 pontos de coordenação e formam uma classe de ligantes quelantes, responsável, por exemplo, pela estabilidade do grupo heme, onde o centro metálico é um íon de ferro.
Assinale a alternativa com as afirmações CORRETAS.