Foram encontradas 260 questões.
Durante um experimento, para a montagem de uma curva de aquecimento do etanol comercial,
com aquecimento uniforme, foi obtido o seguinte gráfico:
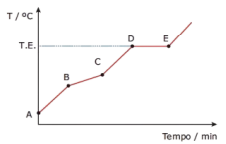
RAGAZZI, M.; GUERRA, F. Mudanças de estado físico e densidade. In: Química. Vol. 1. Belo Horizonte: Editora Bernoulli. p. 13.
Com base na análise do gráfico, é correto afirmar que o etanol comercial

RAGAZZI, M.; GUERRA, F. Mudanças de estado físico e densidade. In: Química. Vol. 1. Belo Horizonte: Editora Bernoulli. p. 13.
Com base na análise do gráfico, é correto afirmar que o etanol comercial
Provas
Questão presente nas seguintes provas
Um técnico de laboratório encontrou um sólido com o rótulo ilegível, ficando em dúvida se o sólido
era cloreto de potássio, sacarose, sílica, nitrato de cálcio ou cloreto de amônio. Para identificar o
material, ele realizou testes de ponto de fusão, de solubilidade em água, de condutividade elétrica
do sólido fundido e de condutividade elétrica em solução. Os resultados indicaram que o sólido
do teste possuía temperatura de fusão relativamente baixa, não conduzia eletricidade nos estados
sólido ou líquido e era solúvel em água.
Com base nessas características, o técnico concluiu que o material era
Com base nessas características, o técnico concluiu que o material era
Provas
Questão presente nas seguintes provas
O hipoclorito de sódio é utilizado como agente oxidante, branqueador e desinfetante em diversas
aplicações industriais e domésticas, sendo produzido através da reação entre cloro gasoso e
solução aquosa de hidróxido de sódio, conforme representado a seguir:
Cl2(g) + NaOH(aq) → NaCl(aq) + NaClO(aq) + H2O(l)
A massa de hidróxido de sódio, em gramas, necessária para a produção de 2,960 toneladas de solução de hipoclorito de sódio 12,5% m/m, é
Dados: Na = 23 g/mol O = 16 g/mol H = 1 g/mol Cl = 35 g/mol
Cl2(g) + NaOH(aq) → NaCl(aq) + NaClO(aq) + H2O(l)
A massa de hidróxido de sódio, em gramas, necessária para a produção de 2,960 toneladas de solução de hipoclorito de sódio 12,5% m/m, é
Dados: Na = 23 g/mol O = 16 g/mol H = 1 g/mol Cl = 35 g/mol
Provas
Questão presente nas seguintes provas
Durante o processo de precipitação para dosagem gravimétrica do cloreto de bário hidratado, o
técnico de laboratório adicionou um excesso de solução diluída de ácido sulfúrico à solução de
cloreto de bário.
O excesso do reagente precipitante tem o objetivo de
O excesso do reagente precipitante tem o objetivo de
Provas
Questão presente nas seguintes provas
- Preparação de Meios de Cultura, Soluções, Reagentes e Corantes
- Controle de Qualidade em Laboratório Clínico
A pureza dos reagentes desempenha um papel importante na exatidão vinculada a qualquer
análise. É, portanto, essencial que a qualidade de um reagente seja consistente com seu propósito
de uso. Em relação às características desejáveis aos reagentes com grau padrão primário, podem
ser citadas:
I) Alta pureza; II) Estabilidade à atmosfera; III) Ausência de água de hidratação; IV) Elevado custo; V) Solubilidade razoável no meio de titulação; VI) Massa molar razoavelmente baixa.
Estão corretas apenas as características
I) Alta pureza; II) Estabilidade à atmosfera; III) Ausência de água de hidratação; IV) Elevado custo; V) Solubilidade razoável no meio de titulação; VI) Massa molar razoavelmente baixa.
Estão corretas apenas as características
Provas
Questão presente nas seguintes provas
- Identificação dos Diversos Equipamentos de um Laboratório, sua Utilização e Conservação
- Vidrarias para Laboratórios
Considere as vidrarias apresentadas no quadro abaixo.
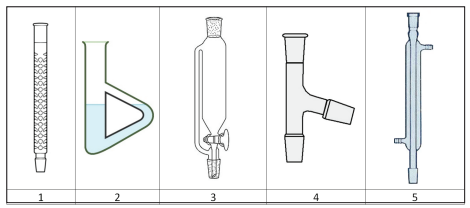
As vidrarias utilizadas em uma montagem de destilação fracionada são

As vidrarias utilizadas em uma montagem de destilação fracionada são
Provas
Questão presente nas seguintes provas
Uma solução foi preparada dissolvendo 4,90 g de ácido sulfúrico em um volume final de 200,00 mL
de solução. Considerando que o ácido sulfúrico utilizado é 100% puro, a concentração normal dessa
solução é igual a
Dados: H = 1 g/mol S = 32 g/mol O = 16 g/mol
Dados: H = 1 g/mol S = 32 g/mol O = 16 g/mol
Provas
Questão presente nas seguintes provas
A análise por Cromatografia em Camada Delgada (CCD) de uma amostra desconhecida, juntamente
com padrões de paracetamol e aspirina em uma mesma cromatoplaca, resultou no seguinte
cromatograma:
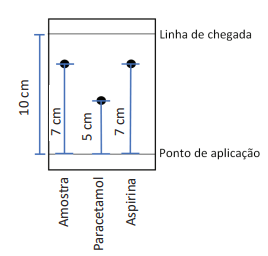
Em relação à interpretação desse cromatograma, é correto afirmar que

Em relação à interpretação desse cromatograma, é correto afirmar que
Provas
Questão presente nas seguintes provas
Um técnico de laboratório, com o objetivo de recuperar o clorofórmio de um resíduo, realizou
uma destilação fracionada da solução. Para confirmar se o produto obtido está de acordo com as
propriedades do reagente puro, ele utilizou a combinação de diversas técnicas simples.
Nesse experimento, a propriedade que NÃO contribui para a identificação do material destilado é a(o)
Nesse experimento, a propriedade que NÃO contribui para a identificação do material destilado é a(o)
Provas
Questão presente nas seguintes provas
Um técnico de laboratório precisou padronizar uma solução de hidróxido de sódio de concentração
teórica igual a 0,100 mol/L, utilizando uma solução de biftalato de potássio de concentração
0,1000 mol/L. Para isso, ele ajustou o menisco de uma bureta de 25,00 mL com a solução de
hidróxido de sódio. Com uma pipeta volumétrica, mediu 10,00 mL da solução do padrão primário
de biftalato de potássio e adicionou, em um erlenmeyer, gotas de uma solução de fenolftaleína
para a visualização do ponto de viragem. O procedimento foi realizado em triplicata, sendo gastos
os seguintes volumes da solução de hidróxido de sódio: 8,10 mL; 8,00 mL e 7,90 mL.
O técnico de laboratório, ao final desse procedimento, concluiu que
O técnico de laboratório, ao final desse procedimento, concluiu que
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container