Foram encontradas 50 questões.
O reservatório de água de um edifício foi desinfetado com cloro. Depois da desinfecção, verificou-se que a água armazenada no tanque continha 15 mg/L de cloro ativo residual. Para reduzir essa quantidade a 5 mg/L, foi providenciada uma decloração da água do tanque, com bissulfito de sódio, segundo a reação descrita a seguir:
NaHSO3 + Cl2 + H2O !$ \rightarrow !$ NaHSO4 + 2HCl
Para se obter a redução da concentração de cloro ativo residual até o valor definido, a quantidade mínima de NaHSO3 consumida será igual a
Provas
O reservatório de água de um edifício foi desinfetado com cloro. Depois da desinfecção, verificou-se que a água armazenada no tanque continha 15 mg/L de cloro ativo residual. Para reduzir essa quantidade a 5 mg/L, foi providenciada uma decloração da água do tanque, com bissulfito de sódio, segundo a reação descrita a seguir:
NaHSO3 + Cl2 + H2O !$ \rightarrow !$ NaHSO4 + 2HCl
Sobre a reação de decloração, é correto afirmar que é um processo em que o
Provas
Para preparar uma solução de KCl, um técnico pesou 74,45 g do sal e transferiu para um balão volumétrico de 1L. Adicionou água para garantir a dissolução e em seguida completou o volume para 1L.
Ao terminar a preparação, o nível de líquido no balão apresentou-se como mostrado na figura a seguir:

Nessas condições, é correto afirmar que a concentração da solução que o técnico preparou é
Provas
Bolsistas de países da América Latina, Caribe e de vários estados brasileiros, participam de um curso promovido pela CETESB, para capacitação de gestão ambiental dos chamados Poluentes Orgânicos Persistentes (POPs). Os POPs são divididos em pesticidas, policlorobifenilos e dioxinas & furanos.
(www.cetesb.sp.gov.br/noticia/482. Acesso em 16.01.2013. Adaptado)
O termo “dioxinas” refere-se, de forma simplificada, a uma família de derivados de dioxina, conhecidos como dibenzodioxinas policlorados, como por exemplo a 2,3,7,8 – tetraclorodibenzo-p-dioxina (I), que tem sido estudada em função da sua toxicidade e efeitos nocivos em animais e seres humanos.
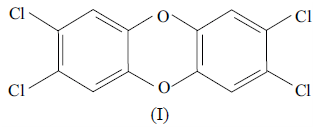
Com base nessas informações, é correto afirmar que a fórmula molecular da dioxina é escrita como
Provas
Na busca de novos métodos de análise para aplicação em triagem de amostras de águas, um técnico de laboratório estudou a reatividade de nitratos metálicos em meio ácido e básico. Em tubos de ensaio contendo soluções aquosas de nitratos metálicos, relacionados na tabelas a seguir, foram adicionadas, gota a gota, cerca de 2 mL de soluções dos reagentes HCl, H2SO4 e NH4OH 30%, separadamente.
|
Sal (solução aquosa 0,2 mol/L) |
|
AgNO3 |
|
Sr(NO3)2 |
|
Mg(NO3)2 |
|
Al(NO3)3 |
|
Pb(NO3)2 |
Considere o gráfico a seguir, que mostra a variação de solubilidade do Al(NO3)3 em função do pH, a 25 ºC.
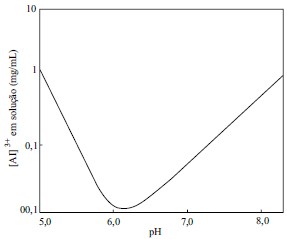
De acordo com o gráfico, para se obter o máximo rendimento na obtenção de Al(OH)3 a partir de uma solução que contém Al(NO3)3, será necessário manter o pH do meio reacional
Provas
Na busca de novos métodos de análise para aplicação em triagem de amostras de águas, um técnico de laboratório estudou a reatividade de nitratos metálicos em meio ácido e básico. Em tubos de ensaio contendo soluções aquosas de nitratos metálicos, relacionados na tabelas a seguir, foram adicionadas, gota a gota, cerca de 2 mL de soluções dos reagentes HCl, H2SO4 e NH4OH 30%, separadamente.
|
Sal (solução aquosa 0,2 mol/L) |
|
AgNO3 |
|
Sr(NO3)2 |
|
Mg(NO3)2 |
|
Al(NO3)3 |
|
Pb(NO3)2 |
Assinale a alternativa que contém, entre as equações apresentadas a seguir, aquela que descreve corretamente a reação que ocorre entre o nitrato de alumínio e o ácido sulfúrico.
Provas
Na busca de novos métodos de análise para aplicação em triagem de amostras de águas, um técnico de laboratório estudou a reatividade de nitratos metálicos em meio ácido e básico. Em tubos de ensaio contendo soluções aquosas de nitratos metálicos, relacionados na tabelas a seguir, foram adicionadas, gota a gota, cerca de 2 mL de soluções dos reagentes HCl, H2SO4 e NH4OH 30%, separadamente.
|
Sal (solução aquosa 0,2 mol/L) |
|
AgNO3 |
|
Sr(NO3)2 |
|
Mg(NO3)2 |
|
Al(NO3)3 |
|
Pb(NO3)2 |
Nas reações realizadas, é correto afirmar que ocorreu formação de precipitado quando o ácido clorídrico foi adicionado aos tubos de ensaio contendo
Provas
Em um laboratório de química, um estagiário localiza em uma parede um sinal como o que está representado a seguir.

Esse sinal indica
Provas
Um técnico de laboratório precisa preparar sulfato de manganês (II) anidro. Para isso, ele vai utilizar sulfato de manganês (II) monoidratado e proceder às seguintes etapas:
1. colocar um cadinho limpo para aquecer sobre a chama de um bico de Bunsen, ajustando o sistema de modo que o cadinho fique posicionado sobre a região mais quente da chama;
2. aquecer por 5 minutos e, em seguida, usando pinças, colocar o cadinho para esfriar sobre a bancada;
3. depois que o cadinho tiver esfriado (temperatura ambiente), pesar e registrar sua massa em milésimos de grama;
4. colocar 1,0 – 1,2 g de sulfato de manganês monoidratado no cadinho, pesar e registrar a massa em milésimos de grama;
5. aquecer por 5 minutos, interromper o aquecimento e repetir os processos descritos nas etapas 2 e 3;
6. repetir a etapa 5 até obter massa constante;
7. tampar o cadinho e, usando pinças e luvas, colocá-lo em um dessecador, até o momento de uso do sulfato de manganês anidro.
Sabendo que foram utilizados 0,165 g de sulfato de manganês monoidratado e que o processo de desidratação foi completo, a massa de sal anidro obtida é igual a
Provas
Um técnico de laboratório precisa preparar sulfato de manganês (II) anidro. Para isso, ele vai utilizar sulfato de manganês (II) monoidratado e proceder às seguintes etapas:
1. colocar um cadinho limpo para aquecer sobre a chama de um bico de Bunsen, ajustando o sistema de modo que o cadinho fique posicionado sobre a região mais quente da chama;
2. aquecer por 5 minutos e, em seguida, usando pinças, colocar o cadinho para esfriar sobre a bancada;
3. depois que o cadinho tiver esfriado (temperatura ambiente), pesar e registrar sua massa em milésimos de grama;
4. colocar 1,0 – 1,2 g de sulfato de manganês monoidratado no cadinho, pesar e registrar a massa em milésimos de grama;
5. aquecer por 5 minutos, interromper o aquecimento e repetir os processos descritos nas etapas 2 e 3;
6. repetir a etapa 5 até obter massa constante;
7. tampar o cadinho e, usando pinças e luvas, colocá-lo em um dessecador, até o momento de uso do sulfato de manganês anidro.
Na figura a seguir, estão representados alguns materiais de uso em laboratórios químicos.
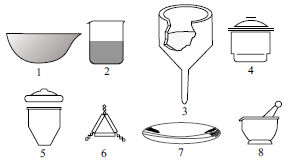
Entre os materiais apresentados na figura, para realizar a prática de acordo com o processo descrito, o técnico utilizará aqueles indicados pelos números
Provas
Caderno Container