Foram encontradas 13.241 questões.
Sobre os métodos de extinção do fogo,
considere suas bases técnicas. Assinale a
alternativa correta:
Provas
Questão presente nas seguintes provas
No Brasil, o processo de fermentação alcoólica constitui a principal rota industrial de produção de etanol.
Em relação à fermentação alcoólica, constata-se que
Provas
Questão presente nas seguintes provas
Nas tintas, as cores claras são cores cujo valor da
coordenada cromática L*, para esmalte, é superior ou
igual a:
Provas
Questão presente nas seguintes provas
Durante o processo de cloração da água em uma ETA,
forma-se ácido hipocloroso (HOCl). Em relação a este
composto, qual afirmação está correta?
Provas
Questão presente nas seguintes provas
Na etapa de coagulação em uma ETA, utiliza-se
frequentemente o sulfato de alumínio Al2(SO4)3. Qual é o
principal mecanismo físico-químico responsável pela
formação de flocos neste processo?
Provas
Questão presente nas seguintes provas
Na cromatografia gasosa, uma amostra de uma mistura que se quer analisar é injetada no instrumento e entra em uma
corrente de gás, chamada de fase móvel, que transporta essa amostra para a coluna de separação. Os componentes
são separados dentro dessa coluna, e o detector mede a quantidade dos componentes que saem da coluna. A
separação dentro da coluna se dá por dois parâmetros: (i) efeito da volatilidade dos compostos, em que os mais
voláteis tendem a passar mais tempo na fase móvel e têm um menor tempo de retenção; (ii) efeito da polaridade, em
que os compostos de maior polaridade tendem a interagir mais fortemente quando utilizada coluna constituída de
material cuja superfície possui natureza polar e têm maior tempo de retenção. Considere uma amostra constituída de
uma mistura dos compostos I a V, cujas estruturas são mostradas na figura a seguir. Essa amostra foi injetada num
instrumento que possui uma coluna de sílica.
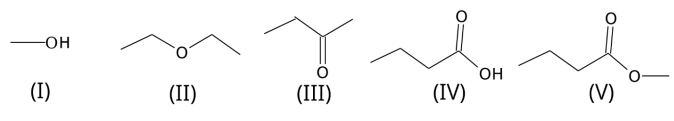
A sequência da saída dos compostos, do menor ao maior tempo de retenção, é:

A sequência da saída dos compostos, do menor ao maior tempo de retenção, é:
Provas
Questão presente nas seguintes provas
O prêmio Nobel de Química de 2025 foi destinado a três pesquisadores pelas suas contribuições à área de redes
metalorgânicas (Metal-Organic Framework – MOF). Esses materiais são promissores em diversas aplicações, como
captura de CO2 e água da atmosfera, catálise e armazenamento de hidrogênio verde. A síntese desses materiais é
relativamente simples; por exemplo, um MOF pode ser preparado ao misturar AlCl3.6H2O com
ácido 3,5-pirazoldicarboxílico (H2DPC, estrutura mostrada na figura) na proporção 1:2 em água e colocado em
autoclave a 180 °C por 12 horas. A reação é determinada por controle termodinâmico, isto é, as interações ácido-base
de Lewis direcionam o produto. Ao término, são obtidas as redes estendidas, cristalinas, porosas, bastante estáveis e
insolúveis do MOF.
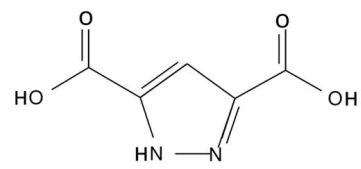
O material mencionado no texto é produzido graças às interações entre:

O material mencionado no texto é produzido graças às interações entre:
Provas
Questão presente nas seguintes provas
A crioterapia é largamente utilizada por atletas para recuperação muscular. Atualmente, existem no mercado
compressas de gelo instantâneas que se baseiam no processo endotérmico da dissolução de nitrato de amônio
(NH4NO3, M = 80 g mol–1) em água (capacidade térmica específica c = 4,2 J g–1 K–1). Essas compressas são bolsas
descartáveis, normalmente de tecido de polipropileno, que contêm inicialmente, em compartimentos separados, água
e o sal de amônio, que, quando misturados, atingem a temperatura de até 0 ºC. A entalpia de dissolução do nitrato de
amônio é um processo que está relacionado à entalpia de rede cristalina (ΔlatH = −646 kJ mol–1) e a entalpias de
hidratação do cátion (ΔhidH = −307 kJ mol–1) e do ânion (ΔhidH = −313 kJ mol–1). Uma compressa possui uma certa massa
de sal de amônio e 200 g de água e está inicialmente a 20 ºC.
Para que a temperatura da compressa atinja 0 ºC (considerando que não há trocas de calor com o tecido nem com o exterior), a massa, em gramas, de sal de amônio no compartimento deve ser mais próxima de:
Para que a temperatura da compressa atinja 0 ºC (considerando que não há trocas de calor com o tecido nem com o exterior), a massa, em gramas, de sal de amônio no compartimento deve ser mais próxima de:
Provas
Questão presente nas seguintes provas
O cloreto de lítio é um importante material utilizado na indústria como precursor de lítio metálico e outros sais e óxidos
empregados na fabricação de baterias para veículos elétricos, smartphones etc. A energia de rede é um parâmetro
fundamental que define várias das propriedades químicas de sais. Esse parâmetro pode ser calculado indiretamente
por meio de valores de entalpia experimentais de reações auxiliares. A seguir, são fornecidos alguns dados
termodinâmicos de reações auxiliares para se determinar a energia de rede do cloreto de lítio.
Entalpia de formação do cloreto de lítio: −408 kJ mol–1 Entalpia de formação do cloreto gasoso: −233 kJ mol–1 Entalpia de formação do cloreto aquoso: −167 kJ mol–1 Entalpia de formação do Li+ aquoso: −278 kJ mol–1 1ª Energia de ionização do lítio: 513 kJ mol–1 Afinidade eletrônica do cloro: 348 kJ mol–1 Entalpia de atomização do lítio: 159 kJ mol–1 Entalpia de atomização do cloro: 121 kJ mol–1
Conforme os dados fornecidos, o valor de energia de rede do sal mencionado é mais próximo de:
Entalpia de formação do cloreto de lítio: −408 kJ mol–1 Entalpia de formação do cloreto gasoso: −233 kJ mol–1 Entalpia de formação do cloreto aquoso: −167 kJ mol–1 Entalpia de formação do Li+ aquoso: −278 kJ mol–1 1ª Energia de ionização do lítio: 513 kJ mol–1 Afinidade eletrônica do cloro: 348 kJ mol–1 Entalpia de atomização do lítio: 159 kJ mol–1 Entalpia de atomização do cloro: 121 kJ mol–1
Conforme os dados fornecidos, o valor de energia de rede do sal mencionado é mais próximo de:
Provas
Questão presente nas seguintes provas
Atualmente, existe uma grande procura por novas tecnologias de conversão de energia. As células a combustível de
metanol direto (DMFCs) são uma promissora tecnologia em que a principal vantagem é a operação em baixa
temperatura e a facilidade de transporte do combustível. Essas células utilizam uma solução de metanol (3 mol L–1)
que reage em uma camada catalítica para formar dióxido de carbono. A água é consumida no ânodo, e os íons H+ são
transportados através da membrana de troca de prótons até o cátodo, onde reagem com o oxigênio para produzir água.
A seguir são mostradas as equações das semirreações desse processo. Os elétrons são transportados por meio de
um circuito externo do ânodo para o cátodo, fornecendo energia aos dispositivos conectados.
CH3OH + H2O → 6 H+ + 6 e− + CO2 (ânodo) O2 + 4 H+ + 4 e− → 2 H2O (cátodo)
Devido às características de operação e restrições, essas células operam com potências de saída da ordem de 0,3 kW. Para um sistema projetado para fornecer 24 V, a corrente que passa pelo circuito é de 12,5 A.
Dado: ℱ = 96.500 C mol–1.
Considerando que o sistema acima descrito opere por um período de 100 horas, qual é o valor mais próximo do volume, em litros, de solução de metanol consumido?
CH3OH + H2O → 6 H+ + 6 e− + CO2 (ânodo) O2 + 4 H+ + 4 e− → 2 H2O (cátodo)
Devido às características de operação e restrições, essas células operam com potências de saída da ordem de 0,3 kW. Para um sistema projetado para fornecer 24 V, a corrente que passa pelo circuito é de 12,5 A.
Dado: ℱ = 96.500 C mol–1.
Considerando que o sistema acima descrito opere por um período de 100 horas, qual é o valor mais próximo do volume, em litros, de solução de metanol consumido?
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container