Foram encontradas 30 questões.
Provas
A velocidade de desintegração radioativa de um radioisótopo é de primeira ordem em relação ao número de núcleos radioativos. Uma amostra contendo 5 g do 222Rn sofreu desintegração radioativa durante 6,6 dias e teve sua massa reduzida para 1,5 g. Calcule o tempo de meia-vida, aproximadamente, em dias, desse radioisótopo.
(Dado: ln 0,30 = –1,2.)
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Provas
Brometo de nitrosila é um gás vermelho que pode ser obtido pela reação do óxido nítrico com bromo molecular, de acordo com a seguinte equação química:
NO(g) + ½ Br2(g) → NOBr(g)
Resultados cinéticos da síntese desse gás estão representados na tabela a seguir:
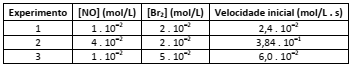
O valor da constante de velocidade da reação de obtenção do brometo de nitrosila, em L2
/mol2 . s, é igual a
Provas
O ciclo de energia global representado no diagrama mostra a variação de entalpia em diversos processos bioquímicos.
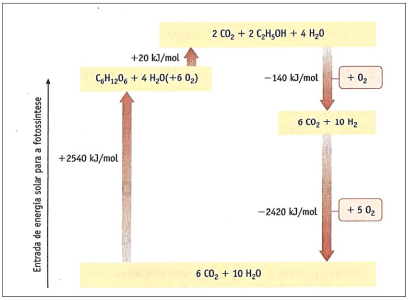
A energia, em kJ, envolvida na produção de um mol de hidrogênio a partir de biomassa é de
Provas
Provas
- Química CinéticaRepresentação das Transformações Químicas
- Química InorgânicaSoluções e Substâncias InorgânicasSubstâncias Inorgânicas: dissociação iônica e ionização, conceitos de ácido-base
Provas
Determine o pH aproximado de uma solução tampão preparada pela adição de 14,5 g de bicarbonato de sódio e 9 g de carbonato de sódio em água suficiente para completar 500 mL de solução.
(Dados: pKa do ácido é 10,32 ; log 2 = 0,3 ; log1/2 = -0,3.)
Provas
O ácido 2-aminopropanoico pode ser representado conforme suas estruturas espaciais a seguir:

Baseado no sistema de nomenclatura de Cahn-Ingold-Prelog assinale a opção que melhor caracteriza o nome das representações anteriores.
Provas
Quando se estudam as diferentes classes de compostos inorgânicos mais comuns, percebe-se que podem ser obtidas em um laboratório de química sem necessidade de aparatos complexos. Como exemplos, abaixo seguem propostas de algumas reações de obtenção de óxidos, ácidos, bases e sais:
I. Pb(NO3)2(s) 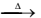 PbO(s) + 2 NO(g) + 1,5 O2(g)
PbO(s) + 2 NO(g) + 1,5 O2(g)
II. CaO(s) + SiO2(S) 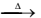 CaSiO3(L)
CaSiO3(L)
III. Cu(s) + H2SO4(conc) → CuSO4(aq) + H2(g)
IV. (NH4)2Cr2O7(s) 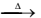 N2(g) + Cr2O3(s) + 4 H2O(L)
N2(g) + Cr2O3(s) + 4 H2O(L)
V. 2 NO2(g) + H2O(L) → HNO3(aq) + HNO2(aq)
VI. Pb(NO3)2(aq) + Fe(s) → não reativa
Das possibilidades de reações químicas apresentadas anteriormente, estão quimicamente corretas, de acordo com os processos de síntese e reatividade dos compostos inorgânicos, apenas
Provas
Caderno Container