Foram encontradas 470 questões.
O cloreto de prata é um sal de baixa solubilidade em água (Kps =
1,8x10-10, a 25°C).
A adição de NH3(aq) a uma solução saturada de cloreto de prata em contato com o precipitado resultará
A adição de NH3(aq) a uma solução saturada de cloreto de prata em contato com o precipitado resultará
Provas
Questão presente nas seguintes provas
A norma ABNT ISO 17025 trata dos requisitos gerais para a
competência de laboratórios de ensaios e calibração. Os
organismos de acreditação, que reconhecem a competência de
laboratórios de ensaio e calibração, devem se basear nessa
norma.
Com relação a esta norma, analise as afirmativas a seguir, assinalando V para as verdadeiras e F para as falsas.
( ) O laboratório deve manter registro de reclamações de clientes, das investigações e ações corretivas implementadas. ( ) O laboratório deve assegurar que condições físicas e ambientais não invalidem os resultados. ( ) O laboratório deve ter e aplicar procedimento para estimar a incerteza da medição de todas as calibrações.
Segundo a ordem apresentada, as afirmativas são, respectivamente,
Com relação a esta norma, analise as afirmativas a seguir, assinalando V para as verdadeiras e F para as falsas.
( ) O laboratório deve manter registro de reclamações de clientes, das investigações e ações corretivas implementadas. ( ) O laboratório deve assegurar que condições físicas e ambientais não invalidem os resultados. ( ) O laboratório deve ter e aplicar procedimento para estimar a incerteza da medição de todas as calibrações.
Segundo a ordem apresentada, as afirmativas são, respectivamente,
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Na utilização de carbonato de sódio como padrão primário foi
pesado 2,650 g de carbonato de sódio anidro PA, previamente
dessecado a 200 °C durante uma hora. Esse sólido foi dissolvido,
num béquer, com água deionizada e transferido para um balão
de 500 mL completando assim esse volume. 10 mL dessa solução
de carbonato de sódio serão utilizados, numa titulação, para
padronizar uma solução 0,1 mol.L-1 de ácido clorídrico com
alaranjado de metila como indicador.
O volume previsto de titulado que deverá ser gasto nesse processo, considerando nenhum tipo de perda será de
Dados: massas molares (g.mol-1) C= 12; O=16; Na= 23.
O volume previsto de titulado que deverá ser gasto nesse processo, considerando nenhum tipo de perda será de
Dados: massas molares (g.mol-1) C= 12; O=16; Na= 23.
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
- Técnicas de LaboratórioEquipamentos e Técnicas Básicas
O gráfico a seguir apresenta a curva de calibração para a
determinação da concentração de fósforo reativo em amostras
de águas doces utilizando o método do ácido ascórbico.
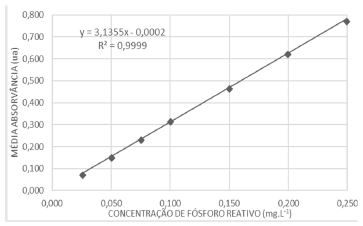
Nas mesmas condições analíticas uma amostra de água doce de um reservatório classe 2 com concentração desconhecida apresentou absorvância média 0,142 ua.
A concentração de fósforo reativo (em mg.L-1) na amostra é, aproximadamente, de

Nas mesmas condições analíticas uma amostra de água doce de um reservatório classe 2 com concentração desconhecida apresentou absorvância média 0,142 ua.
A concentração de fósforo reativo (em mg.L-1) na amostra é, aproximadamente, de
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
A alcalinidade total de uma amostra de 40,00mL da água de um
reservatório foi determinada por titulação utilizando ácido
clorídrico 0,0020 mol.L-1 previamente padronizado. No
procedimento de análise, 3 gotas de solução de fenolftaleína 1%
foram adicionadas a amostra que permaneceu incolor; em
seguida, foram adicionadas 3 gotas de solução de alaranjado de
metila 0,2% e a amostra foi titulada consumindo 7,50 mL do
ácido clorídrico.
A alcalinidade total da amostra, em mgCaCO3.L-1, corresponde aproximadamente a
Dados: massas molares em g.mol-1: C = 12; O = 16; Ca = 40. Equação para a titulação: 2HCl + CaCO3 → CaCl2 + H2O + CO2.
A alcalinidade total da amostra, em mgCaCO3.L-1, corresponde aproximadamente a
Dados: massas molares em g.mol-1: C = 12; O = 16; Ca = 40. Equação para a titulação: 2HCl + CaCO3 → CaCl2 + H2O + CO2.
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
A massa de hidróxido de sódio contida em 100 mL de uma
solução de pH 9 a 25°C é:
Dados: massas molares em g.mol-1 : H = 1; O = 16; Na = 23.
Dados: massas molares em g.mol-1 : H = 1; O = 16; Na = 23.
Provas
Questão presente nas seguintes provas
- Interações com Tecnologia, Sociedade e Meio Ambiente
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
O esgoto doméstico é uma das principais fontes de poluentes
orgânicos despejados nos corpos d’água.
Se a quantidade de matéria orgânica e de microrganismos aeróbios no esgoto for alta, a diminuição da concentração de oxigênio dissolvido no meio provocará alterações no ambiente aquático.
A quantidade de oxigênio necessária para o consumo da matéria orgânica pode ser avaliada em laboratório, utilizando o excesso do reagente
Se a quantidade de matéria orgânica e de microrganismos aeróbios no esgoto for alta, a diminuição da concentração de oxigênio dissolvido no meio provocará alterações no ambiente aquático.
A quantidade de oxigênio necessária para o consumo da matéria orgânica pode ser avaliada em laboratório, utilizando o excesso do reagente
Provas
Questão presente nas seguintes provas
Em um recipiente de volume constante foi efetuada a reação de
decomposição a temperatura constante:
2SO3(g)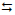 2SO2(g) + O2(g).
2SO2(g) + O2(g).
Inicialmente a pressão parcial do trióxido de enxofre era de 1,6 bar. Ao atingir o equilíbrio foi constatada uma porcentagem de decomposição de 60%.
Se a esse sistema em equilíbrio for adicionado 1 mmol de dióxido de enxofre, mantendo-se constante as condições anteriores, quando o novo equilíbrio for atingido,
2SO3(g)
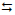 2SO2(g) + O2(g).
2SO2(g) + O2(g).
Inicialmente a pressão parcial do trióxido de enxofre era de 1,6 bar. Ao atingir o equilíbrio foi constatada uma porcentagem de decomposição de 60%.
Se a esse sistema em equilíbrio for adicionado 1 mmol de dióxido de enxofre, mantendo-se constante as condições anteriores, quando o novo equilíbrio for atingido,
Provas
Questão presente nas seguintes provas
Além de serem utilizados para a desinfecção no tratamento de
água, compostos com cloro podem ser usados para controlar o
sabor e o odor. Algumas vezes o sabor ou o odor estão
relacionados com a presença de ácido sulfídrico, matéria orgânica
em decomposição, compostos com ferro e manganês. No
controle do sabor e do odor o cloro pode participar das seguintes
reações:
1) H2S (aq) + 4 Cl2 (aq) + 4 H2O (liq)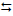 8 HCl (aq) + H2SO4 (aq)
2) 2 Fe(HCO3)2 (aq) + Cl2 (aq) + Ca(HCO3)2 (aq)
8 HCl (aq) + H2SO4 (aq)
2) 2 Fe(HCO3)2 (aq) + Cl2 (aq) + Ca(HCO3)2 (aq) 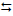 2 Fe(OH)3 (s) + CaCl2
(aq) + 6 CO2 (g)
3) MnSO4 (aq) + Cl2 (aq) + 4 NaOH (aq)
2 Fe(OH)3 (s) + CaCl2
(aq) + 6 CO2 (g)
3) MnSO4 (aq) + Cl2 (aq) + 4 NaOH (aq) 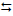 MnO2 (ppt) + 2 NaCl (aq) +
Na2SO4 (aq) + 2H2O (liq)
MnO2 (ppt) + 2 NaCl (aq) +
Na2SO4 (aq) + 2H2O (liq)
Analise as afirmativas a seguir, relacionadas com as reações.
I. Na reação 1, o enxofre sofre oxidação e o cloro é o agente redutor. II. Na reação 2, o ferro sofre oxidação e o cloro sofre redução. III. Na reação 3, o manganês sofre redução e o cloro é o agente oxidante.
Está correto o que se afirma em
1) H2S (aq) + 4 Cl2 (aq) + 4 H2O (liq)
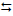 8 HCl (aq) + H2SO4 (aq)
2) 2 Fe(HCO3)2 (aq) + Cl2 (aq) + Ca(HCO3)2 (aq)
8 HCl (aq) + H2SO4 (aq)
2) 2 Fe(HCO3)2 (aq) + Cl2 (aq) + Ca(HCO3)2 (aq) 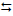 2 Fe(OH)3 (s) + CaCl2
(aq) + 6 CO2 (g)
3) MnSO4 (aq) + Cl2 (aq) + 4 NaOH (aq)
2 Fe(OH)3 (s) + CaCl2
(aq) + 6 CO2 (g)
3) MnSO4 (aq) + Cl2 (aq) + 4 NaOH (aq) 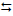 MnO2 (ppt) + 2 NaCl (aq) +
Na2SO4 (aq) + 2H2O (liq)
MnO2 (ppt) + 2 NaCl (aq) +
Na2SO4 (aq) + 2H2O (liq)
Analise as afirmativas a seguir, relacionadas com as reações.
I. Na reação 1, o enxofre sofre oxidação e o cloro é o agente redutor. II. Na reação 2, o ferro sofre oxidação e o cloro sofre redução. III. Na reação 3, o manganês sofre redução e o cloro é o agente oxidante.
Está correto o que se afirma em
Provas
Questão presente nas seguintes provas
O equilíbrio envolvendo os gases N2O4 e NO2 é muito estudado
devido à mudança de coloração das substâncias, o que facilita a
visualização desse processo.
Considere um tubo selado contendo inicialmente N2O4 com pressão parcial de 0,45 atm. e temperatura constante. Após o equilíbrio ser atingido, a pressão parcial determinada para o N2O4 foi de 0,08 atm.
Com base nesses dados experimentais, o valor aproximado da constante de equilíbrio em função das pressões parciais dos gases envolvidos, é de
Considere um tubo selado contendo inicialmente N2O4 com pressão parcial de 0,45 atm. e temperatura constante. Após o equilíbrio ser atingido, a pressão parcial determinada para o N2O4 foi de 0,08 atm.
Com base nesses dados experimentais, o valor aproximado da constante de equilíbrio em função das pressões parciais dos gases envolvidos, é de
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container