Foram encontradas 80 questões.
A matriz de transporte do Brasil está centrada em rodovias, sendo que a principal fonte de energia dos veículos que utilizam esse modal é derivada do petróleo. No entanto, grande parte desse combustível fóssil é constituído por moléculas de cadeias carbônicas muito longas, inviáveis para o uso como combustíveis automotores. As refinarias, assim, contornam esse problema transformando as cadeias longas em moléculas menores pertencentes à fração mais consumida, por meio de um processo químico chamado
Provas
O geraniol é um álcool terpênico insolúvel em água naturalmente encontrado nos óleos essenciais de citronela, gerânio, limão e rosas, entre outras espécies vegetais. Sua molécula contém um grupo funcional álcool, dois carbonos terciários e 18 átomos de hidrogênio.
Considere as estruturas de vários compostos que possuem odores característicos.
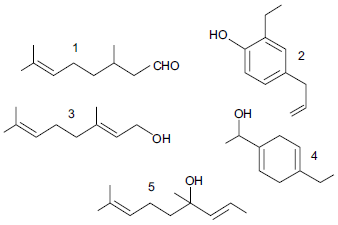
Com base nas informações do texto, o geraniol é representado pela estrutura
Provas
O flúor-18 (18F) é um radioisótopo utilizado em diagnósticos de câncer, com meia-vida igual a 110 minutos, produzido a partir da reação entre núcleos de neônio (20Ne) e o isótopo X, conforme a equação a seguir:
\( ^{20}_{10} Ne + X \rightarrow ^{18}_{9}F+ ^{4}_{2}\alpha \)
O isótopo X e a porcentagem de 18F que resta após 5,5 horas de sua produção são, respectivamente,
Provas
O hipoclorito de sódio (NaC\( \ell \)O) apresenta propriedades bactericidas por promover a oxidação de proteínas, lipídeos e carboidratos existentes nas células bacterianas. A equação mostra a reação entre a glicina e o íon hipoclorito (C\( \ell \)O–).
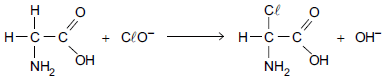
Nessa reação, verifica-se que o átomo de carbono do glicina é pelo íon hipoclorito e o átomo de cloro tem seu número de oxidação alterado de para .
As lacunas do texto são preenchidas, respectivamente, por:
Provas
Segundo a teoria das colisões efetivas, para que uma reação ocorra é necessário que as moléculas dos reagentes colidam umas com as outras com orientação espacial adequada e energia mínima. Assim, qualquer alteração no meio reacional que interfira nesses dois fatores modifica a velocidade da reação. A figura mostra o sistema reacional gasoso 1 submetido a modificações que proporcionaram os sistemas 2 e 3.
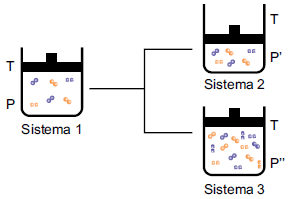
Considerando que as moléculas existentes nesses sistemas reajam entre si, as relações entre as velocidades (V) das reações dos sistemas 1 e 2 e dos sistemas 1 e 3 são, respectivamente,
Provas
Quando ferro metálico é mergulhado em uma solução de ácido clorídrico, ocorre a seguinte reação:
Fe + 2HC\( \ell \) → FeC\( \ell \)2 + H2 \( \Delta H \) = -88 kJ/mol
Considerando o volume molar dos gases igual a 25 L/mol e que em um experimento realizado à temperatura ambiente foram liberados 7,04 kJ de energia, o volume de gás hidrogênio produzido nesse experimento foi de
Provas
O fenômeno da condutividade elétrica de soluções foi explorado pelo químico Svante August Arrhenius em sua tese de doutorado de 1884, intitulada “Pesquisas sobre a Condutividade Galvânica”. Segundo Arrhenius, para que uma substância seja condutora de eletricidade em meio aquoso, deve ser capaz de se dissolver e liberar ou produzir cargas elétricas. Esse comportamento químico é observado nas substâncias
Provas
O ponto de ebulição das substâncias está relacionado com o tipo de interação existente entre suas moléculas e com a massa molecular. O quadro apresenta substâncias com massas moleculares próximas e suas respectivas fórmulas estruturais.

A ordem crescente de temperaturas de ebulição das substâncias apresentadas no quadro é
Provas
Acefato é o nome de um inseticida de fórmula molecular C4H10NO3PS (M = 183 g/mol), indicado para aplicação em culturas de algodão, soja e feijão. A formulação recomendada para uso é de 0,75 a 1 kg dissolvido em 300 a 400 L de água. Assim, a concentração em mol/L da solução mais diluída desse inseticida é igual a
Provas
Os modelos atômicos elaborados ao longo do tempo buscavam explicar fenômenos naturais, alguns dos quais reproduzidos experimentalmente. O modelo proposto por Dalton em 1803, apesar de não explicar muitos dos fenômenos observados na época, contribuiu com a consolidação da
Provas
Caderno Container